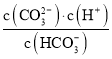题目内容
【题目】NA为阿伏伽德罗常数的值。下列说法正确的是( )
A.1 mol羟基(-OH)中含7NA个电子
B.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
C.50 mL 18.4 mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
D.6.2g白磷(分子式为P4)中所含P—P键的数目为0.2NA
【答案】B
【解析】
A.羟基中电子数为8+1=9,因此1 mol羟基(-OH)中含9NA个电子,故A错误;
B.过氧化钠与水反应中,过氧化钠既是氧化剂,也是还原剂,过氧化钠中氧元素化合价从-1价升高至0价生成氧气,因此生成0.1mol氧气转移的电子数为0.2NA,故B正确;
C.铜与浓硫酸反应随着反应的进行,硫酸浓度逐渐降低,最终反应停止,最终硫酸有剩余,因此无法根据硫酸的物质的量计算最终生成SO2的数目,故C错误;
D.6.2g白磷的物质的量为![]() ,P4的结构为
,P4的结构为![]() ,因此0.05molP4中含有P-P键数目为0.05×6NA=0.3NA,故D错误;
,因此0.05molP4中含有P-P键数目为0.05×6NA=0.3NA,故D错误;
故答案为:B。

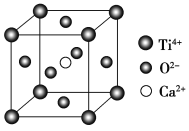
【题目】钙钛矿(主要成分是CaTiO3)太阳能薄膜电池制备工艺简单、成本低、效率高,引起了科研工作者的广泛关注,科学家认为钙钛矿太阳能电池将取代硅基太阳能电池的统治地位。
(1)基态Ti原子的价电子排布式为__,能量最高的能级有__个空轨道;Si、P、S第一电离能由小到大顺序是__。
(2)碳和硅的有关化学键键能如表所示:
化学键 | CC | CH | CO | SiSi | SiH | SiO |
键能/kJmol-1 | 356 | 413 | 336 | 226 | 318 | 452 |
硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是___。
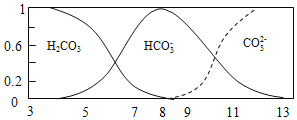
(3)一种新型熔融盐燃料电池以Li2CO3和Na2CO3的熔融盐混合物作电解质,则CO32-的空间构型为___。
(4)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图:
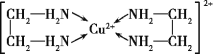
该配离子中含有的化学键类型有__(填字母)。
a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有__个σ键,C原子的杂化方式为__。
(5)CaTiO3的晶胞为立方晶胞,结构如图所示(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶角)Ca2+的配位数为__,与Ti4+距离最近且相等的O2-有__个;晶体的密度为ρg/cm3,最近的Ti4+和O2-之间的距离为__nm(填计算式)。(CaTiO3的摩尔质量为136g/mol,NA为阿伏加德罗常数)。