题目内容
【题目】![]() 、
、![]() 混溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的
混溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的![]()
A. 加入 KSCN的溶液一定不变红色B. 溶液中一定含有![]()
C. 溶液中可能含![]() D. 剩余固体中一定有铜
D. 剩余固体中一定有铜
【答案】B
【解析】
Fe3+的氧化性强于Cu2+,加入铁粉,根据氧化还原反应中先后规律,反应前后Fe+2Fe3+=3Fe2+、Fe+Cu2+=Fe2++Cu或者Cu+2Fe3+=2Fe2++Cu,然后进行分析;
Fe3+的氧化性强于Cu2+,加入铁粉,根据氧化还原反应中先后规律,反应先后先后胡顺序Fe+2Fe3+=3Fe2+、Fe+Cu2+=Fe2++Cu或者Cu+2Fe3+=2Fe2++Cu,
A、因为有固体存在,该固体可能是Fe、Cu的混合物、也可能是Cu,无论哪种哪种情况,得出溶液中一定不含有Fe3+,因此加入KSCN溶液后,溶液不变红,故A说法正确;
B、根据A选项分析,故B说法错误;
C、如果铁粉与Cu2+反应,铁粉不足,溶液中有Cu2+,固体为Cu单质,也符合题意,故C说法正确;
D、根据上述分析,剩余固体中一定含有铜,故D说法正确。

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案【题目】生产中可用双氧水氧化法处理电镀含氰废水,某化学兴趣小组模拟该法探究有关因素对破氰反应速率的影响(注:破氰反应是指氧化剂将CN-氧化的反应)。
【相关资料】
①氰化物主要是以CN-和[Fe(CN)6]3-两种形式存在。
②Cu2+可作为双氧水氧化法破氰处理过程中的催化剂;Cu2+在偏碱性条件下对双氧水分解影响较弱,可以忽略不计。
③[Fe(CN)6]3-较CN-难被双氧水氧化,且pH越大,[Fe(CN)6]3-越稳定,越难被氧化。
【实验过程】
在常温下,控制含氰废水样品中总氰的初始浓度和催化剂Cu2+的浓度相同,调节含氰废水样品不同的初始pH和一定浓度双氧水溶液的用量,设计如下对比实验:
(1)请完成以下实验设计表(表中不要留空格)。
实验序号 | 实验目的 | 初始pH | 废水样品体积/mL | CuSO4溶液的体积/mL | 双氧水溶液的体积/mL | 蒸馏水的体积/mL |
① | 为以下实验操作参考 | 7 | 60 | 10 | 10 | 20 |
② | 废水的初始pH对破氰反应速率的影响 | 12 | 60 | 10 | 10 | 20 |
③ | ________ | 7 | 60 | ______ | ______ | 10 |
实验测得含氰废水中的总氰浓度(以CN-表示)随时间变化关系如图所示。
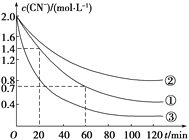
(2)实验①中20~60 min时间段反应速率:v(CN-)=______mol·L-1·min-1。
(3)实验①和实验②结果表明,含氰废水的初始pH增大,破氰反应速率减小,其原因可能是____________________(填一点即可)。在偏碱性条件下,含氰废水中的CN-最终被双氧水氧化为HCO,同时放出NH3,试写出该反应的离子方程式:____________。
(4)该兴趣小组同学要探究Cu2+是否对双氧水氧化法破氰反应起催化作用,请你帮助他们设计实验并验证上述结论,完成下表中内容(已知:废水中的CN-浓度可用离子色谱仪测定) ______。
实验步骤(不要写出具体操作过程) | 预期实验现象和结论 |