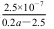题目内容
NOx是汽车尾气中的主要污染物之一。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式: .
(2)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:

①写出该反应的热化学方程式: .
②随温度升高,该反应化学平衡常数的变化趋势是 (填增大、减小或不变)。
(3)在汽车尾气系统中装置催化转化器,可有效降低NO的排放。当尾气中空气不足时,NOX在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式: .
(4)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:

①Pt电极上发生的是 反应(填“氧化”或“还原”)。
②写出NiO电极的电极反应式:
大苏打
【有效成分】Na2S2O3
【规格】l000mL
【质量分数】25%
【密度】1.58g·cm-3
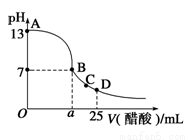
(1)某同学取100 mL该试剂,稀释后使用,稀释后的溶液中c(Na+)=________mol·L-1。
(2)该同学参阅该试剂的配方,欲用Na2S2O3固体配制80 mL与所示试剂物质的量浓度相同的溶液,需要称量Na2S2O3固体的质量为 g;所用到的玻璃仪器有玻璃棒、烧杯、量筒和 。
(3)稀硫酸是重要的化工试剂,某实验小组人员用98%(密度为1.84g·cm-3)的浓硫酸配制2000mL2.3mol·L-1的稀硫酸用于实验。
①所配制的稀硫酸中,H+的物质的量浓度为______mol·L-I。
②需用浓硫酸的体积为 mL。
(4)配置一定物质的量浓度的稀硫酸时,下列操作会使所配溶液物质的量浓度偏低的是
A.定容时俯视容量瓶刻度线 |
B.用量筒量取浓硫酸时俯视刻度线 |
C.容量瓶用蒸馏水洗涤干净后没有干燥就移入所配置溶液 |
D.定容后把容量瓶倒置摇匀,发现液面低于刻度线又加水至刻度线。 |
E.加水时超过刻度线,用胶头滴管吸出
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性环境下易分解生成S和SO2。某小组设计了如下实验装置制备Na2S2O3(夹持及加热仪器略),总反应为2Na2S+Na2CO3+4SO2  3Na2S2O3+CO2。回答下列问题:
3Na2S2O3+CO2。回答下列问题:

(1)装置A的作用是制备______________,反应的化学方程式为______________。
(2)完成下表实验过程:
操作步骤 | 装置C的实验现象 | 解释原因 |
检查装置气密性后,添加药品 | pH计读数约为13 | 用离子方程式表示(以S2-为例): ① |
打开K2,关闭K3,调节K1使硫酸缓慢匀速滴下 | ⅰ.导管口有气泡冒出, ② ⅱ.pH计读数逐渐 ③ | 反应分步进行: Na2CO3+SO2 2Na2S+3SO2 Na2SO3+S |
当pH计读数接近7时,立即停止通SO2,操作是 ④ | 必须立即停止通SO2的原因是: ⑤ |
(3)Na2S2O3有还原性,可作脱氯剂。向Na2S2O3溶液中通入少量Cl2,某同学预测S2O32-转变为SO42-,设计实验验证该预测:取少量反应后的溶液于试管中,______________。
化学在生活中有着广泛的应用,下列对应关系错误的是( )
选项 | 性质 | 实际应用 |
A | SO2具有漂白性 | SO2可用于食品增白 |
B | SiO2熔点高 | SiO2可用于制作耐高温仪器 |
C | Al(OH)3具有弱碱性 | Al(OH)3可用于制胃酸中和剂 |
D | Fe3+具有氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |


 OO-)+ c(OH-)
OO-)+ c(OH-) Si(s)+4HCl(g); △H = + QkJ/mol (Q>0),一定温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是 ( )
Si(s)+4HCl(g); △H = + QkJ/mol (Q>0),一定温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是 ( ) min)
min)