题目内容
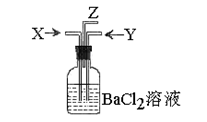
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是

| A.洗气瓶中没有看到明显现象 |
| B.气体X是纯净物 |
| C.洗气瓶中产生的沉淀是碳酸钡 |
| D.Z导管口有红棕色气体出现 |
D
C+2H2SO4 CO2↑+2SO2↑+2H2O 即:X为CO2和SO2混合气体;
CO2↑+2SO2↑+2H2O 即:X为CO2和SO2混合气体;
Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O 即Y为NO2
按题意,将三气体通入氯化钡溶液后:
NO2+SO2=NO+SO3 SO3+H2O=H2SO4 H2SO4+BaCl2=BaSO4↓+2HCl
可知:反应后的溶液呈强酸性,得到不溶于酸的BaSO4沉淀,但不能得到可溶于酸的BaSO3、BaCO3;同时CO2在强酸性溶液中不能存在,和NO一起逸出,而NO在瓶口可被氧化为NO2,而呈现红棕色
 CO2↑+2SO2↑+2H2O 即:X为CO2和SO2混合气体;
CO2↑+2SO2↑+2H2O 即:X为CO2和SO2混合气体;Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O 即Y为NO2
按题意,将三气体通入氯化钡溶液后:
NO2+SO2=NO+SO3 SO3+H2O=H2SO4 H2SO4+BaCl2=BaSO4↓+2HCl
可知:反应后的溶液呈强酸性,得到不溶于酸的BaSO4沉淀,但不能得到可溶于酸的BaSO3、BaCO3;同时CO2在强酸性溶液中不能存在,和NO一起逸出,而NO在瓶口可被氧化为NO2,而呈现红棕色

练习册系列答案
相关题目