题目内容
在1.00 L 1.00 mol·L-1的NaOH溶液中通过16.8 L(标准状况)CO2,计算所得溶液中含有的NaHCO3和Na2CO3的物质的量。
所得溶液中含NaHCO3 0.500 mol,含Na2CO3 0.250 mol。
解析:
此题若用常规的写化学方程式列方程组求解的方法显得极为烦琐。而直接利用反应前后钠离子和碳原子守恒求解,会简捷准确得多。
设所得溶液中含有NaHCO3的物质的量为x,Na2CO3的物质的量为y。
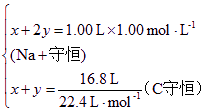
解得![]()

练习册系列答案
相关题目
下图为某市市售盐酸试剂瓶标签上的部分数据。通过计算回答:
(1)在标准状况下,1体积水吸收多少体积的HCl气体可制得此盐酸?(水的密度以1.00 g·cm-3计)
(2)该盐酸25.4 mL与2.00 mol· L-1的NaOH溶液100 mL混合,再将混合后溶液稀释至1.00 L,此时溶液中氢离子的物质的量浓度约为多少?
盐酸 分子式:HCl 相对分子质量:36.5 外观:合格 密度:约为1.18 g·cm-3 HCl的质量分数:36.5% 符合GB622—89 |