题目内容
如图表示298K时N2与H2反应过程中的能量变化.根据图叙述正确的是( )

A.该反应的热化学方程式为:
| ||||
| B.不用催化剂,生成1molNH3放出的热量为46KJ | ||||
| C.加入催化剂,生成1molNH3的反应热减小50KJ?mol-1 | ||||
| D.曲线b表明加入催化剂降低了反应热,加快了反应速率 |

A、该反应放出的能量大于吸收的能量,所以为放热反应,书写热化学方程式要注意化学计量数与反应物物质的量的关系,该反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92kJ?mol-1,故A错误;
B、催化剂对反应热大小无影响,根据选项A可知,生成2molNH3放出92kJ,所以生成 1molNH3放出的热量为46 KJ,故B正确;
C、加入催化剂改变反应速率,不改变化学平衡,反应的热效应不变,故C错误;
D、加入催化剂降低了反应的活化能,反应速率加快,但是反应热不变,故D错误;
故选B.
B、催化剂对反应热大小无影响,根据选项A可知,生成2molNH3放出92kJ,所以生成 1molNH3放出的热量为46 KJ,故B正确;
C、加入催化剂改变反应速率,不改变化学平衡,反应的热效应不变,故C错误;
D、加入催化剂降低了反应的活化能,反应速率加快,但是反应热不变,故D错误;
故选B.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
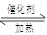 2SO3(g)2 min末测得容器中有7.2 mol SO2。试回答:
2SO3(g)2 min末测得容器中有7.2 mol SO2。试回答: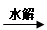 葡萄糖
葡萄糖 CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)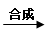 人体所需的蛋白质(人体生长发育、新陈代谢)
人体所需的蛋白质(人体生长发育、新陈代谢)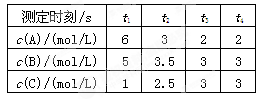
 2C
2C 2Z(g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表: