题目内容
 氢气是一种清洁能源,氢气的制取与利用是氢能源领域的研究热点
氢气是一种清洁能源,氢气的制取与利用是氢能源领域的研究热点已知:CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.2kJ?mol-1
CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJ?mol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法.CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为
(2)上述方法值得的H2可以和CO在一定条件下合成多种有机物,当两者一物质的量1:1催化反应,其原子利用率达100%,合成的物质可能是
a.汽油 b.乙醇 c.甲醛(HCHO) d.乙酸
(3)在一定温度和压强下,CO和H2催化合成二甲醛的反应为:
3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)
若一体积可变的密闭容器中充入3mol H2,3mol CO.1mol CH3,1mol CO2,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍.则:反应开始时正,逆反应速率的大小:v(正)
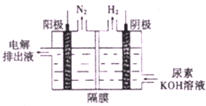
(4)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图如图(电解池中隔膜仅阻止气体通过,阴阳极均为惰性电极),电解时,阳极的电极反应式为
考点:热化学方程式,化学电源新型电池,化学平衡的影响因素
专题:基本概念与基本理论
分析:(1)根据已知的反应和目标反应,利用盖斯定律来计算反应热,并书写热化学反应方程式;
(2)根据质量守恒定律和化合反应的定义和特点判断,主要是利用反应前后原子的种类不变,其数目必保持不变分析判断;
(3)反应前后气体总质量不变;用差量法解题,方程式中3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)减少了4mol;
(4)由阳极排出液中含有大量的碳酸盐成份,则尿素在阳极参与反应,N元素的化合价升高,以此来书写电极反应;利用总反应计算出生成1mol氮气转移的电子的物质的量,再根据电子守恒计算出需要铅的质量.
(2)根据质量守恒定律和化合反应的定义和特点判断,主要是利用反应前后原子的种类不变,其数目必保持不变分析判断;
(3)反应前后气体总质量不变;用差量法解题,方程式中3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)减少了4mol;
(4)由阳极排出液中含有大量的碳酸盐成份,则尿素在阳极参与反应,N元素的化合价升高,以此来书写电极反应;利用总反应计算出生成1mol氮气转移的电子的物质的量,再根据电子守恒计算出需要铅的质量.
解答:
解:(1)①CH4(g)+H2O(g)═CO (g)+3H2(g)△H=+206.2kJ?mol-1,
②CH4(g)+CO2(g)═2CO (g)+2H2(g)△H=+247.4kJ?mol-1,
由盖斯定律可知,①×2-②可得CH4(g)+2H2O(g)═CO2(g)+4H2(g),
其反应热△H=(+206.2kJ?mol-1)×2-(+247.4kJ?mol-1)=+165.0 kJ?mol-1,
即热化学方程式为CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0 kJ?mol-1,
故答案为:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0 kJ?mol-1;
(2)“绿色化学”能实现零排放,即反应物中的原子利用率达到100%,也就是说反应类型一般是化合反应,且反应后产物中的各原子数目比不变,CO和H2在一定条件下按照不同的比例反应,可假定反应时的化学计量数之比为1:1,则只要各选项中的化学式能化为形式(CO)n(H2)n,都是正确的,汽油是烃类的混合物,乙醇(C2H6O)可变为(C2O)1(H2)3,甲醛(CH2O)可变为(CO)1(H2)1,乙酸(C2H4O2)可变为(CO)2(H2)2,
故答案为:cd;
(3)反应前后气体总质量不变,同温、同压下,达到平衡时,气体密度增大,即气体体积缩小,说明平衡向着正向移动,即:v(正)>v(逆);平衡时混合气体密度是同温同压下起始时的1.6倍,则总物质的量变为原先的
=0.625倍,总物质的量=8×0.625=5mol,反应前后减少了3mol,设反应生成甲醚xmol,
3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△n,
1 6-2=4
x 3mol
4x=1×3mol,
解得:x=0.75mol
所以平衡时,n(CH3OCH3)=1+0.75=1.75mol,
故答案为:>; 1.75;
(4)由阳极排出液中含有大量的碳酸盐成份,尿素在阳极参与反应,则阳极反应式为CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O,
由图可知,阴极生成氢气,则阴极反应为6H2O+6e-═3H2↑+6OH-,总反应为CO(NH2)2+2KOH═K2CO3+N2↑+3H2↑,生成1mol氮气转移了6mol电子,铅蓄电池负极材料为Pb,1mol铅完全反应失去2mol电子,所以转移6mol电子需要3molPb,需要Pb的质量为:207g/mol×3mol=621g,
故答案为:CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O;621.
②CH4(g)+CO2(g)═2CO (g)+2H2(g)△H=+247.4kJ?mol-1,
由盖斯定律可知,①×2-②可得CH4(g)+2H2O(g)═CO2(g)+4H2(g),
其反应热△H=(+206.2kJ?mol-1)×2-(+247.4kJ?mol-1)=+165.0 kJ?mol-1,
即热化学方程式为CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0 kJ?mol-1,
故答案为:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0 kJ?mol-1;
(2)“绿色化学”能实现零排放,即反应物中的原子利用率达到100%,也就是说反应类型一般是化合反应,且反应后产物中的各原子数目比不变,CO和H2在一定条件下按照不同的比例反应,可假定反应时的化学计量数之比为1:1,则只要各选项中的化学式能化为形式(CO)n(H2)n,都是正确的,汽油是烃类的混合物,乙醇(C2H6O)可变为(C2O)1(H2)3,甲醛(CH2O)可变为(CO)1(H2)1,乙酸(C2H4O2)可变为(CO)2(H2)2,
故答案为:cd;
(3)反应前后气体总质量不变,同温、同压下,达到平衡时,气体密度增大,即气体体积缩小,说明平衡向着正向移动,即:v(正)>v(逆);平衡时混合气体密度是同温同压下起始时的1.6倍,则总物质的量变为原先的
| 1 |
| 1.6 |
3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△n,
1 6-2=4
x 3mol
4x=1×3mol,
解得:x=0.75mol
所以平衡时,n(CH3OCH3)=1+0.75=1.75mol,
故答案为:>; 1.75;
(4)由阳极排出液中含有大量的碳酸盐成份,尿素在阳极参与反应,则阳极反应式为CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O,
由图可知,阴极生成氢气,则阴极反应为6H2O+6e-═3H2↑+6OH-,总反应为CO(NH2)2+2KOH═K2CO3+N2↑+3H2↑,生成1mol氮气转移了6mol电子,铅蓄电池负极材料为Pb,1mol铅完全反应失去2mol电子,所以转移6mol电子需要3molPb,需要Pb的质量为:207g/mol×3mol=621g,
故答案为:CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O;621.
点评:本题考查了热化学方程式的书写、原电池工作原理、化学平衡的影响因素及计算,题目难度较大,试题题量较大,知识点较多,充分考查了学生对所学知识的掌握情况,试题有利于培养学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温常压下,48g O2和O3组成的混和气体中所含的氧原子数为3NA |
| B、2mol H2O中含有36NA个电子 |
| C、2L 0.1mol?L-1 H2SO4溶液中含有0.2NA个H+ |
| D、常温常压下,22.4L CH4中含有NA个CH4分子 |
用加热的方法可以分离的一组物质是( )
| A、氯化铵和消石灰 |
| B、碳酸氢钠和氯化铵 |
| C、碳酸氢铵和过氧化钠 |
| D、氯化铵和氯化钠 |
对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A、若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
| B、达到化学平衡时,4v正(O2)=5v逆(NO) |
| C、达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 |
| D、化学反应速率关系是:v(正)>v(逆) |
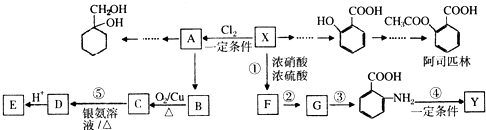
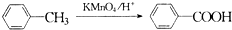
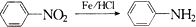 (苯胺,易被氧化)
(苯胺,易被氧化)