题目内容
11.下列中,属于含有共价键的离子化合物的是( )| A. | H2O2 | B. | Br2 | C. | KOH | D. | NaCl |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物,据此分析解答.
解答 解:A.双氧水分子中H-O、O-O原子之间只存在共价键,为共价化合物,故A错误;
B.溴分子中Br-Br原子之间只存在共价键,为单质,故B错误;
C.KOH中钾离子和氢氧根离子之间存在离子键、O-H原子之间存在共价键,为离子化合物,故C正确;
D.氯化钠中钠离子和氯离子之间只存在离子键,为离子化合物,故D错误;
故选C.
点评 本题考查离子化合物和共价化合物判断,侧重考查基本概念,明确物质的构成微粒及微粒之间作用力即可解答,题目难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
6.现有下列短周期元素性质的数据:
试回答下列问题:
(1)元素③在周期表中的位置是第二周期第ⅠA族;元素①②④⑦的气态氢化物中最稳定的是H2O(填化学式);
(2)上述元素形成的单核离子中半径最大的是P3-,半径最小的是Li+;
(3)元素①与元素⑥按照原子个数比为1:1形成的化合物与水反应的化学反应方程式2Na2O2+2H2O═4NaOH+O2↑;
(4)元素⑤形成的单质加入到元素②的氢化物的水溶液中,反应生成两种强酸的离子方程式4Cl2+H2S+4H2O═10H++8Cl-+SO42-.
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或 最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)元素③在周期表中的位置是第二周期第ⅠA族;元素①②④⑦的气态氢化物中最稳定的是H2O(填化学式);
(2)上述元素形成的单核离子中半径最大的是P3-,半径最小的是Li+;
(3)元素①与元素⑥按照原子个数比为1:1形成的化合物与水反应的化学反应方程式2Na2O2+2H2O═4NaOH+O2↑;
(4)元素⑤形成的单质加入到元素②的氢化物的水溶液中,反应生成两种强酸的离子方程式4Cl2+H2S+4H2O═10H++8Cl-+SO42-.
2.核电荷数为1~18的元素中,下列说法正确的是( )
| A. | 最外层只有1个电子的元素一定是金属元素 | |
| B. | 最外层有2个电子的元素一定是金属元素 | |
| C. | 原子核外各层电子数相等的元素一定是金属元素 | |
| D. | 最外层电子数为7的原子,最高正价为+7 |
6.下列各组物质:①Cu和硝酸 ②Cu和氯化铁溶液③Zn和硫酸④Fe和盐酸由于浓度不同而发生不同反应的是( )
| A. | ①③ | B. | ③④ | C. | ①② | D. | ①③④ |
3.下列有关O2的摩尔质量表示正确的是( )
| A. | 32 | B. | 32g | C. | 32mol | D. | 32g/mol |
20.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 4.48L F2变为离子时,获得的电子数为0.2NA | |
| B. | 16g甲烷所含的原子数为NA | |
| C. | 2molNa与足量的O2反应无论是生成Na2O还是Na2O2时电子转移数目为2NA | |
| D. | 18g重水(D2O)所含的电子数为10NA |
1.在一定条件下MO3-与M-发生反应:MO3-+5M-+6H+═3M2+3H2O,则下列关于M元素的叙述中正确的是( )
| A. | M位于元素周期表的第VA族 | B. | M的氢化物的水溶液呈酸性 | ||
| C. | MO3-中的M元素只能被还原 | D. | M2在常温常压下一定是气体 |
 (X为卤素原子)
(X为卤素原子) 的物质,该物质是一种香料.请根据下述路线,回答下列问题:
的物质,该物质是一种香料.请根据下述路线,回答下列问题:
 .
. .
.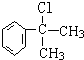 的水解产物
的水解产物 不能经氧化反应⑥而得到产品,导致产率低.
不能经氧化反应⑥而得到产品,导致产率低. 等.
等. (1)某温度下,2L恒容密闭容器中,X、Y、Z三种气体发生化学反应时,物质的量随时间变化的关系曲线如图所示,则
(1)某温度下,2L恒容密闭容器中,X、Y、Z三种气体发生化学反应时,物质的量随时间变化的关系曲线如图所示,则