��Ŀ����
Ҫ����0.2 mol��L��1�Ĵ�����Һ500 mL������ƽ�ϳƳ�________ g̼���ƾ���(Na2CO3��10H2O)���ѳƺõ�̼���ƾ������________�������________ʹ����ȫ�ܽ⣬��ȴ�����£����Ƶõ���Һ��________С�ĵ�ע��________��������ˮϴ���ձ��ڱ�________�Σ�����ÿ��ϴ��Һ��ע��________������������ƿʹ���������Һ��Ͼ��ȣ������ؼ�������ˮ�����ӽ��̶���________ cmʱ������________��ˮ���պúͿ̶���________��������ƿ���ã�����ҡ�ȣ�
������
|
28.6 g,�ձ�,����ˮ,����,500 mL����ƿ,2��3��,����ƿ,1��2,��ͷ�ι�,���� |

��ij��ѧ�С���������ͼ��ʾ�����ּг�װ������ȥ��ʵ��װ�ã���̽����ʪ��Cl2�����Na2CO3 ���巴Ӧ�õ��Ĺ������ʵijɷ֡�
��֪��ͨ��һ�������������D��ֻ��һ�ֳ�����Ϊ�ƺ�ɫ�����壬��Ϊ�������������ȷ������C�й��庬��NaHCO3 ���Һ��ȵ���ֻ��һ�֡��ֶ�C�ijɷֽ��в����̽����

��1������������룺����֪C����0.1molCl2ǡ�ú�10.6��Na2CO3������ȫ��Ӧ����C����Cl2���뷴Ӧ�Ļ�ѧ����ʽ���� ��
��2��������������衣
����1���������ֳɷ֣�NaHCO3�� ��
����2���������ֳɷ֣�NaHCO3�� �� ��
����ƺ���������C�����е�δ֪�ɷֽ���̽������д��ʵ�鲽���Լ�Ԥ������ͽ��ۣ��ɲ���������
��ѡʵ���Լ�������������ˮ��ϡHNO3��Ba(OH)2��Һ��BaCl2��Һ������ʯ��ˮ��AgNO3��Һ���Թܡ�С�ձ���
|
ʵ�鲽�� |
Ԥ������ͽ��� |
|
����1��ȡ����C�й�����Ʒ���Թ��У�������������ˮ���������������ȫ�ܽ⣬Ȼ��������Һ��װA��B��֧�Թ��С� |
|
|
����2�� |
|
|
����3�� |
|
|
|
|
��̽������ʯ�����ĺ�����2. 25g����ʯ��Ʒ��һϵ�л�ѧ�������Ƶ���Ԫ��ȫ��ΪFe2���Ĵ���Һ250 mL�����÷�Ӧ 6Fe2����Cr2O72����14H����6Fe3����2Cr3����7H2O ������ʯ����Ԫ�صĺ������вⶨ��
�������ձ�������������Ͳ����ͷ�ιܣ�Ҫ����0.0150 mol/L K2Cr2O7��Һ100mL������Ҫ�IJ��������� ��
��ȡ25mL����Һ���еζ���ƽ������ K2Cr2O7��Һ���Ϊ25.00 mL��������ʯ����Ԫ�صİٷֺ����ǣ�Fe�����ԭ������Ϊ56�� ��
���ڱ�ʵ��ĵζ������У����в�����ʹ�ⶨ���ƫС���� ����д��ţ���
a��δ�ñ�K2Cr2O7��Һ��ϴ�ζ���
b����ƿ�м��������Һ���ټ�����ˮ
c����ƿ�ڵζ������о���ҡ����������Һ�彦��
 4C (g) ��H >0 �ﵽƽ��ʱ��c(A) ="2" mol��L-1��c ( B) =" 7" mol��L-1��c ( C) =" 4" mol��L-1����ȷ��B����ʼŨ��c (B)��ȡֵ��Χ�� �����ı��������´ﵽƽ�����ϵ��C�����������������д�ʩ���е��� ��
4C (g) ��H >0 �ﵽƽ��ʱ��c(A) ="2" mol��L-1��c ( B) =" 7" mol��L-1��c ( C) =" 4" mol��L-1����ȷ��B����ʼŨ��c (B)��ȡֵ��Χ�� �����ı��������´ﵽƽ�����ϵ��C�����������������д�ʩ���е��� ��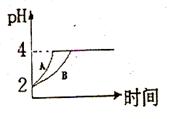
 4C (g) ��H >0 �ﵽƽ��ʱ��c(A) ="2" mol��L-1��c ( B) =" 7" mol��L-1��c ( C) =" 4" mol��L-1����ȷ��B����ʼŨ��c (B)��ȡֵ��Χ�� �����ı��������´ﵽƽ�����ϵ��C�����������������д�ʩ���е��� ��
4C (g) ��H >0 �ﵽƽ��ʱ��c(A) ="2" mol��L-1��c ( B) =" 7" mol��L-1��c ( C) =" 4" mol��L-1����ȷ��B����ʼŨ��c (B)��ȡֵ��Χ�� �����ı��������´ﵽƽ�����ϵ��C�����������������д�ʩ���е��� ��