题目内容
某溶液中只有Na+、CH3COO-、H+、OH-四种离子,且浓度大小的顺序为:
c(CH3COO-)>c(Na+)>c(H+)>c(OH-),该溶液可能是()
c(CH3COO-)>c(Na+)>c(H+)>c(OH-),该溶液可能是()
| A.由0.1mol·L-1的CH3COOH溶液与0.1mol·L-1的NaOH溶液等体积混合而成 |
| B.由10mLpH=3的CH3COOH溶液与1mLpH=11的NaOH溶液混合而成 |
| C.由0.1mol·L-1的CH3COONa溶液与0.1mol·L-1的NaOH溶液等体积混合而成 |
| D.由0.1mol·L-1的CH3COONa溶液与0.1mol·L-1的CH3COOH溶液等体积混合而成 |
D
由题干信息:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),判断溶液显酸性。
A项中混合后生成CH3COONa溶液,显碱性,不选。B项中CH3COOH电离产生的n(H+)=10mL×10-3mol·L-1,大于NaOH电离产生的n(OH-)=1mL×10-3mol·L-1;溶液生成CH3COONa水解显碱性,n(CH3COONa)=1mL×10-3mol·L-1,而剩余n(H+)更多,故B项应为c(CH3COO-)>c(H+)>c(Na+)>c(OH-),不选。C项溶液混合后显碱性,故不选。D项在等物质的量浓度时,弱酸(或弱碱)的电离往往占优势,故选D。
A项中混合后生成CH3COONa溶液,显碱性,不选。B项中CH3COOH电离产生的n(H+)=10mL×10-3mol·L-1,大于NaOH电离产生的n(OH-)=1mL×10-3mol·L-1;溶液生成CH3COONa水解显碱性,n(CH3COONa)=1mL×10-3mol·L-1,而剩余n(H+)更多,故B项应为c(CH3COO-)>c(H+)>c(Na+)>c(OH-),不选。C项溶液混合后显碱性,故不选。D项在等物质的量浓度时,弱酸(或弱碱)的电离往往占优势,故选D。

练习册系列答案
相关题目
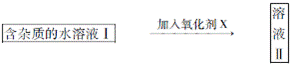
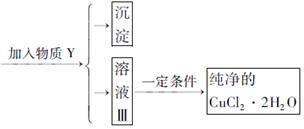
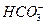
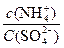 的值是()
的值是() 不可能大量存在
不可能大量存在 、
、 、
、 、
、
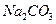 、
、 、
、
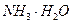 、
、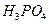 、
、 、
、