题目内容
从海水中提取镁,可按如下步骤进行:① 把贝壳制成石灰乳;② 在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物;③ 将沉淀物与盐酸反应,结晶,过滤、得到含结晶水的晶体;④ 将得到晶体在一定条件下加热得到无水氯化镁;⑤ 电解无水氯化镁,得到金属镁。下列说法中不正确的是
A.此法的优点之一是原料来源丰富
B.①②③ 步骤的目的是从海水中提取 MgCl2
C.以上提取镁的过程中涉及化合、分解和复分解反应
D.以上提取镁的过程中涉及的反应均不是氧化还原反应
D
【解析】
试题分析:① 把贝壳制成石灰乳反应为CaCO3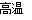 CaO+CO2↑,CaO+H2O=Ca(OH)2. ②Ca(OH)2+ MgCl2 =Mg(OH)2↓+CaCl2. ③Mg(OH)2+2HCl= MgCl2+H2O. ⑤MgCl2
CaO+CO2↑,CaO+H2O=Ca(OH)2. ②Ca(OH)2+ MgCl2 =Mg(OH)2↓+CaCl2. ③Mg(OH)2+2HCl= MgCl2+H2O. ⑤MgCl2 Mg+ Cl2↑.A.由以上化学反应可知制取的原料为贝壳、海水、盐酸。所以原料丰富。正确。B. ①②③ 步骤的目的是从海水中提取纯净的MgCl2。正确。C. CaCO3
Mg+ Cl2↑.A.由以上化学反应可知制取的原料为贝壳、海水、盐酸。所以原料丰富。正确。B. ①②③ 步骤的目的是从海水中提取纯净的MgCl2。正确。C. CaCO3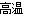 CaO+CO2↑,是分解反应,CaO+H2O=Ca(OH)2是化合反应. Ca(OH)2+MgCl2= Mg(OH)2↓+CaCl2 、Mg(OH)2+2HCl= MgCl2+H2O.是复分解反应,MgCl2
CaO+CO2↑,是分解反应,CaO+H2O=Ca(OH)2是化合反应. Ca(OH)2+MgCl2= Mg(OH)2↓+CaCl2 、Mg(OH)2+2HCl= MgCl2+H2O.是复分解反应,MgCl2 Mg+ Cl2↑是分解反应。故反应类型正确。D MgCl2
Mg+ Cl2↑是分解反应。故反应类型正确。D MgCl2 Mg+ Cl2↑既是分解反应,也是氧化还原反应。所以该选项错误。
Mg+ Cl2↑既是分解反应,也是氧化还原反应。所以该选项错误。
考点:考查制取金属镁的反应原理及海水的综合利用的知识。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目