题目内容
将等物质的量的金属Na、Mg、Al分别与100 mL 2 mol·L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图所示,则下列说法错误的是
| A.x=2.24 |
| B.钠的物质的量为0.2 mol |
| C.反应时,Na、Mg、Al均过量 |
| D.曲线b为Mg与盐酸反应的图像 |
C
解析

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
下列有关化学用语使用不正确的是
A.NH3分子的电子式: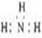 |
| B.N2的结构式: N≡N |
C.O原子的结构示意图: |
D.MgCl2 的电子式: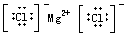 |
设nA为阿伏加德罗常数的数值,下列说法正确的是
| A.1mol Cl2与过量的镁铁反应,转移2nA个电子 |
| B.常温下,16g CH4含有8nA个电子 |
| C.1L 0.5 mol·L-1Na2SO4溶液中含有nA个SO42- |
| D.常温常压下,22.4LCO2含有nA个CO2分子 |
将8.34 g FeSO4·7H2O样品隔绝空气加热脱水,其热重曲线(样品质量随温度变化的曲线)如右
图所示。则下列说法不正确的是
| A.在100℃时,M的化学式为FeSO4·4H2O |
| B.FeSO4·7H2O晶体中有4种不同结合力的水分子 |
| C.FeSO4·H2O存在的最高温度为373℃ |
D.380℃的P加热至650℃时的化学方程式为:2FeSO4 Fe2O3+SO2↑+SO3↑ Fe2O3+SO2↑+SO3↑ |
下列溶液中NO3-的浓度与500 mL 0.4 mol·L-1 KNO3溶液中NO3-的浓度相等的是
| A.50 mL 4 mol·L-1的KNO3溶液 |
| B.1 L 0.2 mol·L-1的KNO3溶液 |
| C.100 mL 0.2 mol·L-1的Ba(NO3)2溶液 |
| D.500 mL 0.4 mol·L-1的Ba(NO3)2溶液 |
一定体积的溶质质量分数为14%的氢氧化钾溶液,若将其蒸发掉50 g水后,其溶质的质量分数恰好增大1倍,溶液体积变为62.5 mL。则浓缩后溶液的物质的量浓度为
| A.2.2 mol·L-1 | B.4 mol·L-1 |
| C.5 mol·L-1 | D.6.25 mol·L-1 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.25 ℃时,pH=12的Ba(OH)2溶液中含有的OH-数目为0.02NA |
| B.室温下,14.0 g乙烯和丁烯的混合气体中含有C—H键数目为2.0NA |
| C.1 L 0.5 mol·L-1的(NH4)2SO4溶液中含有的NH数目为NA |
| D.标准状况下,22.4 L CCl4中含有共用电子对数目为4.0NA |
在一定温度下,已知有关某溶液的一些数据:①溶液的质量 ②溶剂的质量 ③溶液的体积 ④溶质的摩尔质量 ⑤溶质(气体)的体积(Vm已知) ⑥溶液的密度 ⑦溶液的质量分数。利用下列各组数据计算该溶液的物质的量浓度,不能算出的一组是
| A.③⑤ | B.②④⑤⑥ | C.①④⑥ | D.①②③④ |
实验中需用2.0 mol·L-1的Na2CO3溶液950 mL,配制时应选用容量瓶的规格和称取Na2CO3固体的质量分别为 ( )。
| A.950 mL;201.4 g | B.1 000 mL;212.0 g |
| C.100 mL;21.2 g | D.500 mL;100.7 g |