题目内容
11.已知有如图物质相互转化试回答:
(1)写出B的化学式FeCl2,D化学式KCl
(2)C溶液的溶质中含有的化学键是离子键、共价键
(3)写出由E转变成F的化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3
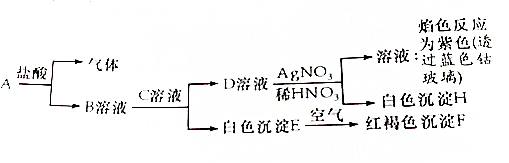
分析 D与硝酸酸化的硝酸银溶液产生白色沉淀H,则D中含有氯离子,H是AgCl,所得溶液焰色反应呈紫色,则溶液中含有钾离子,根据元素守恒知,D为KCl,白色沉淀E空气中转化为红褐色沉淀F,则E是Fe(OH)2,F是Fe(OH)3,B和C发生复分解反应生成KCl和Fe(OH)2,且A与盐酸反应生成B与气体,可推知B为FeCl2,A是Fe,C为KOH,据此解答.
解答 解:D与硝酸酸化的硝酸银溶液产生白色沉淀H,则D中含有氯离子,H是AgCl,所得溶液焰色反应呈紫色,则溶液中含有钾离子,根据元素守恒知,D为KCl,白色沉淀E空气中转化为红褐色沉淀F,则E是Fe(OH)2,F是Fe(OH)3,B和C发生复分解反应生成KCl和Fe(OH)2,且A与盐酸反应生成B与气体,可推知B为FeCl2,A是Fe,C为KOH.
(1)由上述分析可知,B的化学式为FeCl2,D化学式为KCl,故答案为:FeCl2;KCl;
(2)C为KOH,含有的化学键是:离子键、共价键,故答案为:离子键、共价键;
(3)由E转变成F是Fe(OH)2被氧气氧化生成氢氧化铁,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评 本题考查了无机物的推断,以物质的特殊颜色、焰色反应为突破口采用正逆相结合的方法来进行推断,难度中等.

练习册系列答案
相关题目
1.若含有双键、叁键或环,该分子就不饱和,具有一定的“不饱和度”.其数值可表示为:
不饱和度(Ω)=双键数+叁键数×2+环数.例如: Ω=2.则有关下面有机物
Ω=2.则有关下面有机物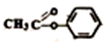 的说法正确的是( )
的说法正确的是( )
不饱和度(Ω)=双键数+叁键数×2+环数.例如:
 Ω=2.则有关下面有机物
Ω=2.则有关下面有机物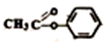 的说法正确的是( )
的说法正确的是( )| A. | 不饱和度为5 | |
| B. | 含有的官能团有碳碳双键和酯基 | |
| C. | 该有机物可以发生水解反应,不能发生氧化反应 | |
| D. | 该有机物所有原子都在同一平面上 |
2.下列除去杂质的方法(括号里为少量杂质)中,所用试剂或操作不正确的是( )
| A. | NaHCO3溶液(Na2CO3):通入过量的CO2 | |
| B. | CO2(HCl):将气体通过盛有饱和Na2CO3溶液的洗气瓶 | |
| C. | SiO2(Al2O3):加入稀盐酸再过滤 | |
| D. | FeCl3溶液(FeCl2):通入足量的氯气 |
19.下列关于分子间作用力的说法,正确的是( )
| A. | 分子间作用力是一种比较弱的化学键 | |
| B. | 氯化钠晶体中不存在范德华力 | |
| C. | 锂、钠、钾、铷、铯的熔点越来越低是因为分子间作用力越来越弱 | |
| D. | 分子间作用力越大,分子的热稳定性就越大 |
6.下列说法正确的是( )
| A. | SO3溶解于水时能导电,所以SO3是电解质 | |
| B. | 离子化合物中不存在独立的分子 | |
| C. | 稀硝酸能导电,所以HNO3溶液属于电解质 | |
| D. | 熔融时能导电的物质一定是电解质 |
16.下列变化中,一定伴随着化学变化的是( )
| A. | 加热碘,收集到紫黑色固体 | |
| B. | 将NaCl固体溶于水后离子键被破坏 | |
| C. | 将CCl4加入溴水中,观察到CCl4成橙色 | |
| D. | 将H2O2滴加在MnO2中,可收集到无色气体 |
3.如图所示为4种氨基酸的结构式,则夏利叙述正确的是( )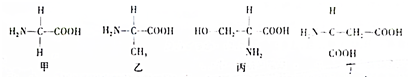
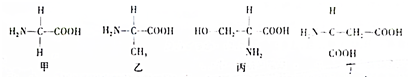
| A. | 构成氨基酸的元素只有C、H、O、N4种 | |
| B. | 氨基酸丙和丁的R基分别是-NH3和-CH2-COOH | |
| C. | R基中可以有氨基或羧基 | |
| D. | 组成水稻的氨基酸包括必需氨基酸和非必需氨基酸 |
15.下列各组物质中,符合前者为混合物,后者为单质的是( )
| A. | Na2CO3•10H2O Na2CO3 | B. | 冰水混合物 液氮 | ||
| C. | 石油 液氢 | D. | 碘酒 干冰 |
16.对于反应A(g)+3B(g)═2C(g),下列各数据表示不同条件下的反应速率,其中反应进行的最快的是( )
| A. | v(A)=0.01mol•L-1•s-1 | B. | v(B)=0.02mol•L-1•s-1 | ||
| C. | v(B)=1.7mol•L-1•min-1 | D. | v(C)=1.0mol•L-1•min-1 |