题目内容
键能是指破坏(或形成)1mol化学键所吸收(或放出)的能量。现查得:H-H、Cl-Cl和H-Cl的键能分别为436kJ/mol、243kJ/mol和431kJ/mol,请用此数据估计,由Cl2、H2生成1molHCl时的热效应为( )
| A.放热91.5kJ | B.放热183kJ | C.吸热183kJ | D.吸热91.5kJ |
A
试题分析:化学反应中,旧键断裂吸收能量,形成新键放出能量。反应Cl2+H2=2HCl中,形成1molHCl时,需要断裂0.5molCl-Cl键和0.5molH-H键,则吸收能量:0.5mol×436KJ/mol+0.5mol×243KJ/mol=339.5KJ,生成1molHCl时需形成1molH-Cl键,放出431KJ能量,则放出的能量为431KJ-339.5KJ=91.5KJ,选A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 O2(g)===4CO2(g)+5H2O(l) ΔH=-2 878 kJ·mol-1
O2(g)===4CO2(g)+5H2O(l) ΔH=-2 878 kJ·mol-1 O2(g)===4CO(g)+5H2O(l) ΔH=-1 746 kJ·mol-1
O2(g)===4CO(g)+5H2O(l) ΔH=-1 746 kJ·mol-1 O2(g)
O2(g) CO(g)的反应热为l10.5kJ/mol,说明碳的燃烧热为110.5kJ/mol
CO(g)的反应热为l10.5kJ/mol,说明碳的燃烧热为110.5kJ/mol
 2S03(g)的能量变化,该反应的ΔH=A一BkJ/mol
2S03(g)的能量变化,该反应的ΔH=A一BkJ/mol HCOOCH3(g)+2H2(g) △H>0
HCOOCH3(g)+2H2(g) △H>0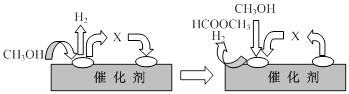


 CO2(g)+H2(g),等物质的量的CO(g)和H2O(g)加入密闭容器中反应,平衡时测得结果如下表。
CO2(g)+H2(g),等物质的量的CO(g)和H2O(g)加入密闭容器中反应,平衡时测得结果如下表。