题目内容
【题目】常温下,下列叙述正确的是( )
A.pH值等于5的HCl溶液和PH值等于9的NaOH溶液由水电离出的c(H+)之比为1:1
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
C.PH=2的HNO3溶液和PH=10的Ba(OH)2溶液等体积混合后的溶液的PH=7
D.向0.1 mol/L的氨水中加入少量醋酸铵固体,则溶液中c(OH-)/c(NH3·H2O)增大
【答案】A
【解析】
A.常温下,pH等于5的HCl溶液和pH值等于9的NaOH溶液由水电离出的c(H+)均为10-9mol/L,故A正确;
B. 醋酸的浓度越大其电离程度越小,所以两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1>10c2,故B错误;
C.pH=2的HNO3溶液和pH=10的Ba(OH)2溶液等体积混合后HNO3过量,pH<7,故C错误;
D.氨水中加入醋酸铵固体,平衡向左移动,c(OH-)减小、c(NH3·H2O)增大,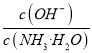 减小,D错误;
减小,D错误;
故答案选A。

练习册系列答案
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
【题目】下表各组物质中,可以实现X![]() Y
Y![]() Z(每步只发生一个反应)所示转化的是( )
Z(每步只发生一个反应)所示转化的是( )
选项 | X | Y | Z | M |
A | Fe | FeCl2 | FeCl3 | HCl |
B | C | CO2 | CO | O2 |
C | CO2 | NaHCO3 | Na2CO3 | NaOH |
D | AlO2- | Al(OH)3 | Al3+ | CO2 |
A.AB.BC.CD.D