题目内容
【题目】把在空气中久置的铝片 5.0 g投入盛有500mL0.5mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如下图的坐标曲线来表示,下列推论错误的是( )
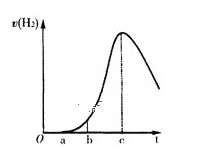
A.t由0→a段不产生氢气是因为表面的氧化物隔离了铝和硫酸溶液
B.t由b→c段产生氢气的速率增加较快的主要原因之一是反应放热温度升高
C.t=c时反应处平衡状态
D.t>c产生氢气的速率降低主要原因是溶液中c(H+)降低
【答案】C
【解析】
A.因铝的表面有一层致密的Al2O3能与HCl反应得到盐和水,无氢气放出,发生的反应为Al2O3+6HCl=2AlCl3+3H2O,故A正确;
B.在反应过程中,浓度减小,反应速率减小,但反应放热,溶液温度升高,反应速率加快,且后者为主要因素,故B正确;
C.反应不是化学平衡,随反应进行反应放热对速率的影响比浓度减少的影响大,当t=c时温度影响最大,t>c时温度影响不是主要因素,浓度减少是主要因素,故C错误;
D.随着反应的进行,溶液中的氢离子浓度逐渐降低,所以反应速率逐渐减小,,故D正确;
故选:C。

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目