题目内容
甲、乙、丙三种金属各1mol与足量稀硫酸反应,产生氢气的物质的量之比为1:2:3,已知甲金属1mol与酸反应产生氯气0.5mol,求这三种金属的化合价.
考点:根据化学式判断化合价,化学方程式的有关计算
专题:计算题
分析:运用电子得失守恒,先根据甲金属1mol与酸反应产生氯气0.5mol,可知甲的化合价为+1价,然后根据甲、乙、丙三种金属各1mol与足量稀硫酸反应,产生氢气的物质的量之比为1:2:3,即化合价之比为1:2:3,求出化合价.
解答:
解:甲金属1mol与酸反应产生氯气0.5mol,根据电子得失守恒可知甲的化合价为+1价,甲、乙、丙三种金属各1mol与足量稀硫酸反应,产生氢气的物质的量之比为1:2:3,即化合价之比为1:2:3,则乙、丙的化合价分别为+2,+3价.
答:三种金属的化合价分别为:+1、+2、+3价.
答:三种金属的化合价分别为:+1、+2、+3价.
点评:本题主要考查了化合价的确定,注意电子得失守恒的运用.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、在高温条件下,C能置换出SiO2中的Si,说明C的非金属性比Si强 |
| B、单质硅是将太阳能转化为电能的常用材料 |
| C、熔融烧碱不能使用石英坩埚和陶瓷坩埚 |
| D、置换反应一定是氧化还原反应,不一定是离子反应 |
在2A+B═3C+4D反应中,表示该反应速率最快的是( )
| A、v(A)=0.5 mol?L-1?s-1 |
| B、v(B)=0.3 mol?L-1?s-1 |
| C、v(C)=0.7 mol?L-1?s-1 |
| D、v(D)=1 mol?L-1?s-1 |
对于合成氨反应:3H2(g)+N2(g)?2NH3(g)△H<0的四个图示,描述不正确的是( )
A、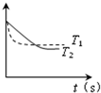 恒容条件下,已知该图中温度T1>T2,则纵轴可表示正反应速率 |
B、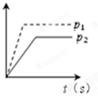 恒温下,已知该图中压强p1>p2,则纵轴可表示NH3的体积分数 |
C、 恒温、恒容下,该图中虚线表示开始充入2mol N2和3mol H2,实线表示开始充入1mol N2和3mol H2,则纵轴可表示H2的转化率 |
D、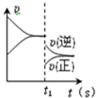 该图可表示平衡后,t1时在恒温恒压下充入He气时正、逆反应速率的变化曲线 |
下列实验操作能达到实验目的是( )
A、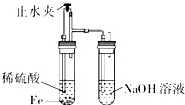 氢氧化亚铁的制备 |
B、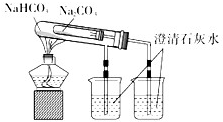 比较Na2CO3、NaHCO3的热稳定性 |
C、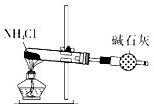 实验室制备少量氨气 |
D、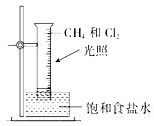 甲烷的取代反应 |