��Ŀ����
����Ŀ���ش���������
(1)������һ�ֿɷ�����硢�ŵ��װ�á���һ�������ڳ��ͷŵ�ʱ�����ķ�Ӧ���£�NiO2+Fe+2H2O![]() Fe(OH2+Ni(OH)2��
Fe(OH2+Ni(OH)2��
�ٴ������ڳ��ʱ����ظ���Ӧ����ӵ�Դ��___�����ӣ��缫��ӦʽΪ____��
�ڷŵ�ʱ����Ni(OH)2��һ�����ڳ��ʱ����___(������������ԭ��)��Ӧ��
(2)����ͼ��ʾװ�ý������в�ͬ�IJ�����
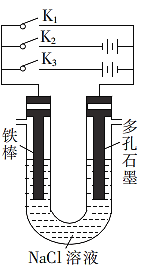
��K1��K2��K3��ֻ�ر�һ���������ĸ�ʴ����������ֻ�պ�___(����K1����K2������K3������ͬ)ʱ��Ϊ�������ĸ�ʴ��Ӧֻ__�պϣ��÷�������Ϊ___
��ֻ�պ�K1����������������5.6gʱ��ʯī�缫���ĵ��������Ϊ_____L(��״��)��
���𰸡��� Fe(OH2+2e-=2OH-+ Fe ���� K2��K3 K2 ��ӵ��������������� 1.12
��������
��1�������ڳ��ʱ��ԭ��صĸ�������ӵ�Դ�ĸ�������������������������������ԭ��Ӧ�������ڳ��ʱ��ԭ��ص���������ӵ�Դ�����������������ص�����������������Ӧ��
��2�����������ص�������ʴ������죬�����ص����������������������ʴ�������������õ�·����������ʧ������Ƚ��м��㡣
��1���������ڳ��ʱ��ԭ��صĸ�������ӵ�Դ�ĸ�������������������������������ԭ��Ӧ����ӦʽΪ��Fe(OH)2+2e-=2OH-+ Fe��
�ڷŵ�ʱ����Ni(OH)2��һ��Ϊԭ��ص����������ʱ�ǵ��أ�Ni(OH)2��һ��������������������Ӧ��
��2����ֻ�պ�K1ʱ��Fe��ԭ��صĸ������ӿ�Fe�ĸ�ʴ��ֻ�պ�K2ʱ��Fe�����ص�������Fe���������÷���Ϊ��ӵ�����������������ֻ�պ�K3ʱ��Fe�����ص��������ӿ�Fe�ĸ�ʴ�����ǵ��ص���������Ľ�����ʴ���ʱ�ԭ��صĸ�������Ľ�����ʴ���ʿ졣��K1��K2��K3��ֻ�ر�һ���������ĸ�ʴ����������ֻ�պ�K3��Ϊ�������ĸ�ʴ��Ӧֻ�պ�K2���÷�������Ϊ��ӵ�����������������
��ֻ�պ�K1������һ��ԭ���װ�ã�Fe����������ʴ��������Ӧʽ��Fe-2e-= Fe2+��������ӦʽΪ��O2+4e-+2H2O![]() 4OH-����������������5.6gʱ����ʧȥ0.2mol e-��������������ʧ��������ȣ�������O2�����ʵ���Ϊ0.05mol���ʱ�״��������O2�����Ϊ0.05mol��(22.4L/mol)=1.12L ��
4OH-����������������5.6gʱ����ʧȥ0.2mol e-��������������ʧ��������ȣ�������O2�����ʵ���Ϊ0.05mol���ʱ�״��������O2�����Ϊ0.05mol��(22.4L/mol)=1.12L ��

����Ŀ����֪����Ӧ����I2(aq)+I-(aq)![]() I3-(aq) ��H1����Ӧ���� I3-(aq)
I3-(aq) ��H1����Ӧ���� I3-(aq) ![]() I2(aq)+I-(aq) ��H2����Ӧ�ٵĻ�ѧƽ�ⳣ��K1���¶ȵĹ�ϵ���±���
I2(aq)+I-(aq) ��H2����Ӧ�ٵĻ�ѧƽ�ⳣ��K1���¶ȵĹ�ϵ���±���
t/�� | 5 | 15 | 25 | 35 | 50 |
K1 | 1100 | 841 | 680 | 533 | 409 |
��ش�
(1)����Ӧ�ڵĻ�ѧƽ�ⳣ��ΪK2������ͬ�¶��£�K1��K2=____________��
(2)������Ӧ�ٵ���H1_______0(����>������=������<��)���������¶ȣ���I2���ܽ����ʻ�______(�����ӿ�����������������������)��
(3)���жϷ�Ӧ���Ѵﵽƽ���������_______________
A�������е�ѹǿ���ٸı� B����Һ����ɫ���ٸı�
C��I-Ũ�Ȳ��ٱ仯 D�����淴Ӧ���ʾ�Ϊ0
(4)ij�¶��£���Ӧ�ٵĻ�ѧƽ�ⳣ��Ϊ800���ڸ��¶��£���ס��ҡ������������зֱ����I2��I-�����������ʵ���ʼŨ�����£�
��ʼŨ��(mol/L) | �� | �� | �� |
c(I2) | 0.1 | 0.2 | 0.2 |
c(I-) | 0.2 | 0.1 | 0.2 |
��Ӧ����������_____________(������������������������)��ƽ��ʱI2��ת����������__________(������������������������)��
����Ŀ�������̿��Ʊ�������ص���Ҫ��Ӧ���£�
�������� 3MnO2+KClO3+6KOH![]() 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O
�����绯 3K2MnO4+2CO2=2KMnO4+MnO2��+2K2CO3
��֪������ʵ��ܽ�ȣ�20����
���� | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
�ܽ��g/100g | 111 | 33.7 | 11.1 | 6.34 |
���������գ�
��1����ʵ���ҽ�������������������ʱ��Ӧѡ������������ǯ��______________��������ţ�
a�������� b�������� c�������� d��������
��2����������᪻���ʱ�����������ԭ����__________�������������ԭ����____________����Ӧ֮��õ�������صIJ����ǣ����ˡ������ᾧ�����ȹ��ˡ��ò����ܹ��õ�������ص�ԭ����____________��
��3�����õ�ⷨҲ��ʵ��K2MnO4��ת����2K2MnO4+2H2O![]() 2KMnO4+2KOH+H2������ԭ������ȣ���ⷨ������Ϊ_________________��
2KMnO4+2KOH+H2������ԭ������ȣ���ⷨ������Ϊ_________________��
��4�������Ƶζ����ⶨ������ص����������������£�
��֪�漰���ķ�Ӧ��
Na2C2O4+H2SO4=H2C2O4(����)+Na2SO4 ��
5H2C2O4+ 2MnO4��+6H+=2Mn2++10CO2��+ 8H2O
Na2C2O4��ʽ����134 KMnO4��ʽ����158��
��.��ȡ0.80 g �ĸ�����ز�Ʒ�����50mL��Һ��
��.��ȡ0.2014 gNa2C2O4��������ƿ�У���������ˮʹ���ܽ⣬�ټ������������ữ��
��.��ƿ����Һ���ȵ�75��80�����������������Ƶĸ��������Һ�ζ����յ㡣���ĸ��������Һ8.48mL��
a.�жϴﵽ�ζ��յ�ı�־��____________________________��
b.��Ʒ�и�����ص���������Ϊ______________������3λС������
c.�����¶ȴ���90�������ֲ��ᷢ���ֽ⣬�ᵼ�²�ò�Ʒ����__________��������ƫ��������ƫ����������Ӱ������
d.��һ�������������Һ���ữ�IJ�������Һ��ϣ���÷�Ӧ��Һ��Mn2+��Ũ���淴Ӧʱ��t�ı仯��ͼ����ԭ�����Ϊ_______________��