题目内容
11.①在淀粉碘化钾溶液中,滴加少量稀硝酸溶液,立即会看到溶液变蓝色,反应的离子方程式是6I-+2NO3-+8H+═2NO↑+3I2+4H2O.②在碘和淀粉形成的蓝色溶液中,通入二氧化硫气体,发现蓝色逐渐消失,反应的离子方程式为I2+SO2+2H2O═2I-+SO42-+4H+.
③对比①和②实验所得的结果,将I2、NO3-、SO42-按氧化性由强到弱顺序排列NO3->I2>SO42-.
分析 ①硝酸根离子在酸性环境下具有强的氧化性,能氧化碘离子生成单质碘;
②碘与二氧化硫反应生成碘化氢、硫酸;
③依据同一氧化还原反应中氧化剂氧化性大于氧化产物氧化性判断解答.
解答 解:①硝酸根离子在酸性环境下具有强的氧化性,能氧化碘离子生成单质碘,离子方程式:6I-+2NO3-+8H+═2NO↑+3I2+4H2O;
故答案为:6I-+2NO3-+8H+═2NO↑+3I2+4H2O;
②在碘和淀粉形成的蓝色溶液中通入SO2气体,二氧化硫被碘单质氧化,同时碘单质被还原成碘离子,溶液蓝色消失,反应的离子方程式:I2+SO2+2H2O═2I-+SO42-+4H+,
故答案为:I2+SO2+2H2O═2I-+SO42-+4H+;
③同一氧化还原反应中氧化剂氧化性大于氧化产物,依据6I-+2NO3-+8H+═2NO↑+3I2+4H2O,氧化性:NO3->I2;
依据I2+SO2+2H2O═2I-+SO42-+4H+,可知氧化性:I2>SO42-;
故答案为:NO3->I2>SO42-.
点评 本题考查了I2、NO3-、SO42-氧化性强弱关系,涉及离子方程式的书写及氧化性强弱判断,明确反应实质是解题关键,注意氧化性、还原性强弱规律,题目难度不大.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
1.活性氧化锌用作橡胶硫化的活性剂、补强剂.以氧化锌粗品为原料制备活性氧化锌的生产工艺流程如下:
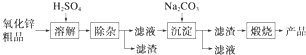
一些阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
(1)“溶解”前将氧化锌粗品粉碎成细颗粒,目的是增大固液接触面积,加快溶解时的反应速率.
(2)“溶解”后得到的酸性溶液中含有Zn2+、SO4 2-,另含有Fe2+、Cu2+等杂质.先加入Na2CO3(填“Na2CO3”或“H2SO4”)调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH)3,同时KMnO4转化为MnO2.经检测溶液中Fe2+的浓度为0.009mol•L-1,则每升溶液中至少应加入0.003mol KMnO4.
(3)杂质Cu2+可利用置换反应除去,应选择的试剂是锌粉.
(4)“沉淀”得到ZnCO3•2Zn(OH)2•H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为ZnCO3•2Zn(OH)2•H2O$\frac{\underline{\;450-500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.

一些阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | Fe(OH)2 |
| pH | 3.2 | 6.7 | 8.0 | 9.7 |
(2)“溶解”后得到的酸性溶液中含有Zn2+、SO4 2-,另含有Fe2+、Cu2+等杂质.先加入Na2CO3(填“Na2CO3”或“H2SO4”)调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH)3,同时KMnO4转化为MnO2.经检测溶液中Fe2+的浓度为0.009mol•L-1,则每升溶液中至少应加入0.003mol KMnO4.
(3)杂质Cu2+可利用置换反应除去,应选择的试剂是锌粉.
(4)“沉淀”得到ZnCO3•2Zn(OH)2•H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为ZnCO3•2Zn(OH)2•H2O$\frac{\underline{\;450-500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.
2.一定条件下的反应aA(g)+bB(g)?cC(g)+dD(g)在一密闭容器中进行,测的反应平均速率2V(A)═3V(D),若该反应过程中气体的物质的量一直保持不变,则a、b、c、d的数值可以是( )
| A. | 2 2 1 3 | B. | 3 1 2 2 | C. | 6 1 2 4 | D. | 2 3 2 3 |
19.下列叙述错误的是( )
| A. | 任何可逆反应都有一定的反应限度 | B. | 反应达到限度即停止了 | ||
| C. | 化学反应限度与时间的长短无关 | D. | 化学反应限度是可以改变的 |
6.下列物质中所有原子一定在同一平面上的是( )
| A. | 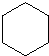 | B. |  | C. | 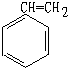 | D. |  |
3.X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,R与Y处于同一主族,Z是短周期中金属性最强的金属元素,W的最高价氧化物对应水化物能与Z、R的最高价氧化物对应水化物均反应生成盐和水.下列说法正确的是( )
| A. | 元素Y、Z、W离子具有相同的电子层结构,其半径依次增大 | |
| B. | 元素X与元素Y能形成两种化学键类型完全相同的化合物 | |
| C. | 元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR | |
| D. | 元素X、Z形成化合物的电子式可以表示成.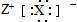 |
20.下列有关化学用语或名称正确的是( )
| A. |  名称:2-甲基乙醇 名称:2-甲基乙醇 | B. | 丙烷分子的比例模型: | ||
| C. | 四氯化碳分子的电子式: | D. | CH4Si的结构式: |
1.有关油脂的下列说法正确的是( )
| A. | 油脂是高级脂肪酸和甘油形成的酯,属纯净物 | |
| B. | 油脂都不能与溴水反应 | |
| C. | 油脂的硬化属于酯化反应 | |
| D. | 天然油脂没有恒定的熔沸点 |