��Ŀ����
����Ŀ��������Ҫ����Ƥ�ë�ġ��ߵ�ֽ�š�Ⱦ�ϵ���ҵ���������ƴ�������ˮâ��(Na2SO4)-̿�ۻ�ԭ����������ʾ��ͼ���£�

��1�������������������������A���뾭�� (��д��������)��������������������������������Ϊ�����ʵ�����CO��CO2��д������ʱ�������ܵĻ�ѧ��Ӧ����ʽΪ ��
��2�����������в���ϡ��Һ������ˮ���ã������� ��
��3��ȡ���ƾ���(������NaOH)���뵽����ͭ��Һ�У���ֽ��衣����Ӧ������Һ��pH��4�����ʱ��Һ��c( S2��)�� ��(��֪������ʱCuS��Cu(OH)2��Ksp�ֱ�Ϊ8.8��10��36��2.2��10��20)
��4����Ƥ�﹤ҵ��ˮ�еĹ��������Ƴ�ȥ������ȥ��������Һ��pH��x(x�������Ƶ�ʵ�����������������ı�ֵ)�й�(����ͼ��ʾ)��Ϊʹ����Ч����ѣ�Ӧ���Ƶ������� �� ��

��ijë�ij���ˮ�к�0.001 mol��L��1�����ƣ���ֽ��Ư��ķ�ˮ(��0.002 mol��L��1 NaClO)��1:2������Ȼ�ϣ���ͬʱ�Ϻô������ַ�ˮ��������ķ�ˮ����������Ҫ�������� ��
���𰸡�
��1�����ˡ����3Na2SO4+8C![]() 3Na2S+4CO2��+4CO��
3Na2S+4CO2��+4CO��
��2����ˮ��ٽ�Na2Sˮ�⣬��ϡ��Һ������Na2Sˮ��
��3��4��10��16
��4���� x��12 pH����9~10֮�� ��SO42����Cl��
��������
�����������1�����ڹ���A�Ǵ�Һ���л�ã����Եõ�A�IJ����ǹ��ˡ��������������ʱ���������̿�ۣ��ҹ���A���Է��벢�������յ�Ӧ�ÿ�֪A��̿�ۣ���ѧʽΪC���������Ϣ��֪�������г��������������һ����̼�Ͷ�����̼������Ӧ���������ƺ�̼����������ʱһ����̼�Ͷ�����̼�ķ��Ӹ�������1��1�����Կ�����������Ļ�ѧ�������ֱ���1��1���ɵø÷�Ӧ�ķ���ʽΪ��![]() Na2SO4 + 2C
Na2SO4 + 2C ![]()
![]() Na2S + 1CO2�� + 1CO�����÷�Ӧ����ͬ����4���õķ�Ӧ����ʽΪ��3Na2SO4 + 8C
Na2S + 1CO2�� + 1CO�����÷�Ӧ����ͬ����4���õķ�Ӧ����ʽΪ��3Na2SO4 + 8C ![]() 3Na2S + 4CO2�� + 4CO�����ʴ�Ϊ�����ˡ����3Na2SO4+8C
3Na2S + 4CO2�� + 4CO�����ʴ�Ϊ�����ˡ����3Na2SO4+8C![]() 3Na2S+4CO2��+4CO����
3Na2S+4CO2��+4CO����
��2�����������в���ϡ��Һ������ˮ���ã�������Һ��������ˮ���Լ��ԣ�ˮ����������ȷ�Ӧ�����ȴٽ�ˮ����У�ϡ����Һ��������ˮ������ã��ʴ�Ϊ����ˮ��ٽ�Na2Sˮ�⣬��ϡ��Һ������Na2Sˮ�⣻
��3��ȡ���ƾ���(������NaOH)���뵽����ͭ��Һ�У���ֽ��裮����Ӧ������Һ��pH = 4������ʱCuS��Cu(OH)2��Ksp�ֱ�Ϊ8.8 �� 10-36��2.2 �� 10-20��Ksp = c(Cu2+) �� c2(OH-) = 2.2 �� 10-20��pH = 4��c(OH-) = 10-10mol/L��c(Cu2+) = 2.2mol/L����ͭ�е�Ksp = c(Cu2+)c(S2-) = 8.8 �� 10-36������õ�c(S2-) = 4 �� 10-36mol/L���ʴ�Ϊ��4 �� 10-36��
��4��������ͼ�������߷�������ȥ�������PH��x��ȡֵ��x=12 pH����9��10֮��ʱ����ȥ������ӽ�100%���ʴ�Ϊ��x=12 pH����9��10֮��
��ijë�ij���ˮ�к�0.001molL-1�����ƣ���ֽ��Ư��ķ�ˮ(��0.002molL-1 NaClO)��1��2������Ȼ�ϣ���ͬʱ�Ϻô������ַ�ˮ���������ƺ����Ʒ���������ԭ��Ӧ��n(Na2S)��n(NaClO) = 0.001 mol/L �� 1��0.002 molL-1 �� 2 = 1��4�����ݵ����غ������֪��Na2S+4NaClO=Na2SO4+4NaCl��������ķ�ˮ����������Ҫ��������SO42-��Cl-���ʴ�Ϊ��SO42-��Cl-��

 ���ɶ���ܲ��¿�ֱͨ�п�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�п�ϵ�д�����Ŀ��������һ�����ױ��ж������ױ����������ױ����֣��������ںϳɸ���Ⱦ�ϡ�ij̽��С���������з�Ӧ��װ���Ʊ�һ�����ױ���
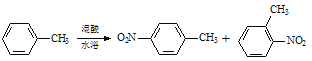
ʵ���п����õ������ݣ�
�ܶ�/gcm-3 | �е�/ �� | �ܽ��� | |
�ױ� | 0.866 | 110.6 | ������ˮ�������������ױ� |
�������ױ� | 1.286 | 237.7 | ������ˮ��������Һ̬�� |
�������ױ� | 1.162 | 222 | ������ˮ��������Һ̬�� |
ʵ�鲽�裺��Ũ������Ũ���ᰴ�����1:3���ƻ����Һ�������ᣩ��40 mL��
��������ƿ�м���13g�ױ����ӷ�������ͼ��ʾװ��ҩƷ������������
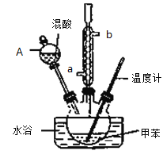
��������ƿ�м�����
�ܿ���ˮԡ�¶�ԼΪ50������Ӧ��Լ10 min������ƿ���д�������ɫ��״Һ����֣�
�ݷ����һ�����ױ������ᴿ���յõ�������һ�����ױ���15 g��
��ش��������⣺
��1��ʵ��ǰ��Ҫ������ƿ�м������� ��Ŀ���� ��
��2�������ܵ������� ����ȴˮ�������ܵ�_______���a����b�����˽��롣
��3������A�������� ��ʹ�ø�����ǰ������еIJ�����_________________��
��4�����뷴Ӧ�����ķ������£�

���У�����1������Ϊ ������2����IJ��������оƾ��ơ��¶ȼơ���ƿ��ţ�ǹܣ�β�ӹܣ��� �� ��
��5����ʵ����һ�����ױ��IJ���Ϊ ��������λ��Ч���֣���



