题目内容
10.下列叙述正确的是( )| A. | 用铂丝蘸取碳酸钾溶液,在火焰上灼烧时呈紫色 | |
| B. | 透过蓝色钴玻璃观察火焰呈紫色,说明该溶液中只含K+ | |
| C. | 现代化学分析测试中常用到元素分析仪、红外光谱仪、原子吸收光谱等 | |
| D. | 焰色反应是化学变化 |
分析 A、K元素的紫色,应通过蓝色的钴玻璃来观察;
B、蓝色钴玻璃能滤去黄光;
C、元素分析仪可以确定物质中含有哪些元素,原子吸收光谱仪确定物质中含有哪些金属元素;
D、焰色反应中没有新的物质生成,属于物理变化;
解答 解:A、玻璃中含有钠元素,洁净的玻璃棒蘸取碳酸钾溶液在酒精灯火焰上灼烧看不到K元素的紫色,应通过蓝色的钴玻璃观察,故A错误.
B、蓝色钴玻璃能滤去黄光,故透过蓝色钴玻璃观察火焰呈紫色,说明该溶液中一定含K+,但还可能含钠离子,故B错误;
C、元素分析仪可以确定物质中含有哪些元素,红外光谱仪可以确定物质中含有的化学键,原子吸收光谱仪确定物质中含有哪些金属元素,故C正确;
D、焰色反应是元素具有的性质,该反应中没有新的物质生成,不属于不会变化,故D错误;
故选C.
点评 本题考查了焰色反应等基础性知识,题目难度中等,注意明确焰色反应为物理变化.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20. 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关粒子的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关粒子的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )
 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关粒子的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关粒子的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )| A. | 当V[NaOH(aq)]=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| B. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大 | |
| C. | H2A第一步电离的方程式为H2A=HA-+H+ | |
| D. | 向NaHA溶液加入水稀释的过程中,pH可能增大也可能减小 |
18.下列关于钠原子和钠离子的叙述正确的是( )
| A. | 钠离子比钠原子少了一个质子 | |
| B. | 钠原子有还原性,钠离子有氧化性 | |
| C. | 钠原子和钠离子有相似的化学性质 | |
| D. | 钠原子不稳定,钠离子稳定,两者具有相同的电子层数 |
15.具有相同质子数的两种粒子( )
| A. | 一定是同种元素 | B. | 一定是一种分子和一种离子 | ||
| C. | 一定是不同离子 | D. | 无法判断 |
19.一定条件下,体积为1L的密闭容器中发生如下反应:SiF4(g)+2H2O(g)?SiO2(s)+4HF(g)△H=+148.9kJ•mol-1
(1)下列各项中能说明该反应已达化学平衡状态的是bcd(填字母序号).
a.v消耗(SiF4)=4v生成(HF)
b.容器内气体压强不再变化
c.容器内气体的总质量不再变化
d.HF的体积分数不再变化
(2)反应过程中测定的部分数据如下表(表中t2>t1)所示.
通过a或b的值及化学平衡原理说明t1时反应是否达到化学平衡状态:t1时反应已经达到化学平衡状态.
(3)若只改变一个条件使上述反应的化学平衡常数变大,该反应ade(填序号).
a.一定向正反应方向移动
b.一定向逆反应方向移动
c.一定是减小压强造成的
d.一定是升高温度造成的
e.SiF4的平衡转化率一定增大.
(1)下列各项中能说明该反应已达化学平衡状态的是bcd(填字母序号).
a.v消耗(SiF4)=4v生成(HF)
b.容器内气体压强不再变化
c.容器内气体的总质量不再变化
d.HF的体积分数不再变化
(2)反应过程中测定的部分数据如下表(表中t2>t1)所示.
| 反应时间/min | n(SiF4)/mol | n(H2O)/mol |
| 0 | 1.20 | 2.40 |
| t1 | 0.80 | a |
| t2 | b | 1.60 |
(3)若只改变一个条件使上述反应的化学平衡常数变大,该反应ade(填序号).
a.一定向正反应方向移动
b.一定向逆反应方向移动
c.一定是减小压强造成的
d.一定是升高温度造成的
e.SiF4的平衡转化率一定增大.
20.中草药秦皮中含有的七叶树内酯结构是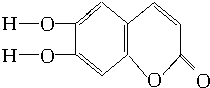 (C、H原子未画出,每个折点表示一个C原子),具有抗菌作用.若1mol的七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗溴水和NaOH的物质的量分别为( )
(C、H原子未画出,每个折点表示一个C原子),具有抗菌作用.若1mol的七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗溴水和NaOH的物质的量分别为( )
 (C、H原子未画出,每个折点表示一个C原子),具有抗菌作用.若1mol的七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗溴水和NaOH的物质的量分别为( )
(C、H原子未画出,每个折点表示一个C原子),具有抗菌作用.若1mol的七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗溴水和NaOH的物质的量分别为( )| A. | 3 mol Br2、2 mol NaOH | B. | 3 mol Br2、4 mol NaOH | ||
| C. | 2 mol Br2、3 mol NaOH | D. | 4 mol Br2、4 mol NaOH |
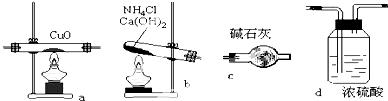 实验室用氨气在加热下还原氧化铜的方法铜的相对原子质量如果选用测定反应物氧化铜和生成物水的质量[m(CO)、m(H2O)]时,如图所示请用下列仪器设计一个简单实验方案.
实验室用氨气在加热下还原氧化铜的方法铜的相对原子质量如果选用测定反应物氧化铜和生成物水的质量[m(CO)、m(H2O)]时,如图所示请用下列仪器设计一个简单实验方案.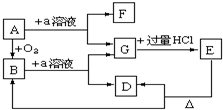 在下列物质的转化关系中,A是一种固体单质,E是一种白色沉淀,F是最轻的气体单质,据此填写下列空白:
在下列物质的转化关系中,A是一种固体单质,E是一种白色沉淀,F是最轻的气体单质,据此填写下列空白: