题目内容
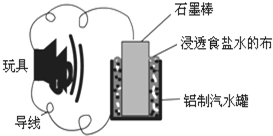 利用生活中常见的材料可以进行很多科学实验,如图就是一个用废旧材料制作的可用于驱动玩具的电池示意图.当电池工作时,有关说法正确的是( )
利用生活中常见的材料可以进行很多科学实验,如图就是一个用废旧材料制作的可用于驱动玩具的电池示意图.当电池工作时,有关说法正确的是( )| A、铝罐将逐渐被腐蚀 |
| B、石墨棒应与玩具电机的负极相连 |
| C、石墨棒上发生的反应为:O2+2H2O-4e-═4OH- |
| D、该电池工作一段时间后石墨棒的质量会减轻 |
考点:化学电源新型电池
专题:电化学专题
分析:石墨棒、铝罐和食盐水构成了原电池,较活泼的金属铝作负极,导电的非金属石墨棒作正极,负极上铝失电子发生氧化反应,正极上得电子发生还原反应;原电池放电时,正极应与玩具电机的正极相连.
解答:
解:A、石墨棒、铝罐和食盐水构成了原电池,较活泼的金属铝作负极,铝失电子生成铝离子,所以铝罐逐渐被腐蚀,故A正确;
B、石墨棒作原电池的正极,所以应与玩具电机的正极相连,故B错误;
C、石墨棒、铝罐和食盐水构成了原电池,导电的非金属石墨棒作正极,正极上氧气得电子生成氢氧根离子,其电极反应式为:O2+2H2O+4e-═4OH-,故C错误;
D、在原电池工作时,石墨棒作正极,电极反应式为O2+2H2O+4e-=4OH-,由此可知石墨棒的质量不会改变,故D错误.
故选A.
B、石墨棒作原电池的正极,所以应与玩具电机的正极相连,故B错误;
C、石墨棒、铝罐和食盐水构成了原电池,导电的非金属石墨棒作正极,正极上氧气得电子生成氢氧根离子,其电极反应式为:O2+2H2O+4e-═4OH-,故C错误;
D、在原电池工作时,石墨棒作正极,电极反应式为O2+2H2O+4e-=4OH-,由此可知石墨棒的质量不会改变,故D错误.
故选A.
点评:本题考查了原电池原理,难度不大,注意把握原电池中正负极的判断方法和电极方程式的书写.

练习册系列答案
相关题目
900℃时,向2.0L恒容密闭容器中充入0.40mol乙苯,发生反应为:
 ?
? (g)+H2(g)△H=a kJ?mol-1.
(g)+H2(g)△H=a kJ?mol-1.
经一段时间后达到平衡.反应过程中测定的部分数据见下表:
下列说法正确的是( )
 ?
? (g)+H2(g)△H=a kJ?mol-1.
(g)+H2(g)△H=a kJ?mol-1.经一段时间后达到平衡.反应过程中测定的部分数据见下表:
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(乙苯)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
| n(苯乙烯)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
| A、反应在前20min的平均速率为v(H2)=0.008mol?L-1?min-1 |
| B、保持其他条件不变,升高温度,平衡时,c(乙苯)=0.08mol?L-1,则a<0 |
| C、保持其他条件不变,再向容器中充入0.40mol乙苯和0.40mol H2,平衡不移动 |
| D、达平衡状态的标志是气体密度不再变化 |
下列分散系不属于胶体的是( )
| A、淀粉溶液 | B、有色玻璃 |
| C、饱和食盐水 | D、肥皂水 |
元素X的单质及X与Y形成的化合物能按如图所示的关系发生转化(其中m≠n,且均为正整数).下列说法正确的是( )


| A、X、Y不可能均为非金属元素 |
| B、若X为Fe,Y只能为Cl |
| C、X一定为金属元素 |
| D、若X为Fe.Y可为Cl、Br,但不能是I |
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)
2N2(g)+3H2O(g)△H<0在恒容的密闭容器中,下列有关说法不正确的是( )
| 180℃ |
| 催化剂 |
| A、每转化掉1mol NO和1mol NO2混合气体,反应转移6mol电子 |
| B、升高温度,可使该反应的反应速率增大 |
| C、平衡时,其他条件不变,升高温度则该反应的平衡常数减少 |
| D、其他条件不变,使用高效催化剂平衡会发生移动,氮氧化物的转化率增大 |
某有机物完全燃烧只生成CO2和H2O,两者的物质的量之比为2:3,可以说( )
| A、该有机物中含C、H、O三种原子 |
| B、该化合物是乙烷 |
| C、该化合物中C、H原子个数比为1:3 |
| D、该化合物分子中含2个C原子、6个H原子,但一定不含有O原子 |
工业生产中常将两种或多种金属(或金属与非金属)在同一容器中加热使其熔合,冷凝后得到具有金属特性的熔合物--合金.这是制取合金的常用方法之一.根据下表数据判断,不宜用上述方法制取合金的是( )
| 金属 | Na | Al | Cu | Fe |
| 熔点(℃) | 97.81 | 660 | 1083 | 1535 |
| 沸点(℃) | 883 | 2200 | 2595 | 3000 |
| A、Fe-Cu合金 |
| B、Cu-Al合金 |
| C、Al-Na合金 |
| D、Cu-Na合金 |