题目内容
【题目】葡萄酒中的酒精是葡萄果实中的糖发酵后的产物(C6H12O6![]() 2CH3CH2OH+2CO2↑)。
2CH3CH2OH+2CO2↑)。
Ⅰ、已知:实验室制乙烯原理为CH3CH2OH![]() CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。
CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。
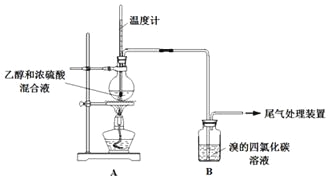
实验操作和现象:
操 作 | 现 象 |
点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 |
…… | |
实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(1)溶液“渐渐变黑”,说明浓硫酸具有 性。
(2)分析,甲认为是C2H4,乙认为不能排除SO2的作用。
①根据甲的观点,使B中溶液褪色反应的化学方程式是 ;
②乙根据现象认为实验中产生的SO2和 ,使B中有色物质反应褪色。
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色。
乙:用下列装置按一定顺序与A连接:(尾气处理装置略)
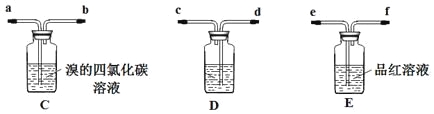
现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色。
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是 ;乙设计的实验D中盛放的试剂是 ,装置连接顺序为 。
b.能说明确实是SO2使E中溶液褪色的实验是 。
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是 。由此可得出的干燥的SO2不能使Br2的四氯化碳溶液褪色
Ⅱ、葡萄酒中常用Na2S2O5做抗氧化剂。
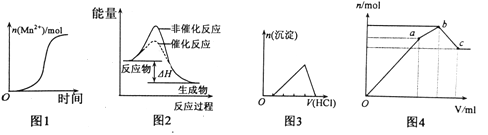
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化如图所示。写出Na2S2O5溶于水时发生的化学方程式 。

(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7。把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-5mol·L-1],此时溶液中c(SO32-)≤ mol·L-1。
【答案】(1)脱水性(1分)(2)①CH2=CH2+ Br2→ CH2Br—CH2Br(1分)②H2O (1分)③a.NaOH 溶液(1分)浓硫酸(1分)(d)cabe(f)(2分)b.加热已经褪色的品红溶液,若红色恢复,证明是SO2使品红溶液褪色而不是Br2(2分)c.SO2+ 2H2O +Br2="=" 4H++2Br-+ SO42- 、SO42- + Ba2+="=" BaSO4↓或SO2+ 2H2O +Br2+ Ba2+="=" 4H++ 2Br-+ BaSO4↓(2分)(3)Na2S2O5+H2O=2NaHSO3(1分) 0.05(2分)
【解析】
试题(1)溶液慢慢变黑是因为浓硫酸将物质中的C和H以1:2的比例脱掉,所以表现浓硫酸的脱水性。
(2)①甲认为是C2H4,使B中溶液褪色是因为发生加成反应,反应的化学方程式是CH2=CH2+ Br2→ CH2Br—CH2Br;②乙根据现象认为浓硫酸同时可能被还原生成SO2和水;③a.甲设计实验中A、B间洗气瓶中盛放NaOH 溶液,将二氧化硫吸收,再通过Br2的CCl4溶液如若褪色,则说明是乙烯加成;将A中出来的气体通过浓硫酸除去水,再通过溴的四氯化碳,不褪色,再通过品红褪色,故连接为cabe(f);b.利用二氧化硫漂白的不稳定性,加热已经褪色的品红溶液,若红色恢复,证明是SO2使品红溶液褪色而不是Br2;c. ,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是SO2+ 2H2O +Br2="=" 4H++2Br-+ SO42- 、SO42- + Ba2+="=" BaSO4↓。
(3)溶液的pH=4.5时,溶液中主要存在HSO3-,故Na2S2O5溶于水时发生的化学方程式:Na2S2O5+H2O=2NaHSO3。
(4)因为Ksp[BaSO4]=1×10-10,c(SO42-)≤1×10-5mol·L-1,故c(Ba2+)≥1×10-5mol·L-1,Ksp[BaSO3]=5×10-7,故c(SO32-)≤0.05 mol·L-1。

 口算题天天练系列答案
口算题天天练系列答案【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:

苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了______气体。该反应为_______(填“吸热”或“放热”)反应,冷却水流向是_____________(填“上进下出”或“下进上出”),继续滴加至液溴滴完。其中仪器c的名称是________,其作用是:__________________________________。装置d的作用是:_____________________________________________________;烧瓶中发生的有机反应的方程式为:_______________________________________________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL 10%的NaOH溶液、10mL水洗涤。洗涤、分离有机和无机试剂,需要用到的仪器是:_____________。第一次水洗除去大部分的HBr;用NaOH溶液洗涤的作用是______________;第二次水洗的目的是:____________;每一次洗涤,有机层从_________(填“下口放出”或“上口倒出”),棕黄色的溴苯经过提纯后恢复为无色。
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_____________。
(3)经以上分离操作后,粗溴苯中还含有的主要杂质苯,要进一步提纯,下列操作中必须的是____(填入正确选项前的字母)。
A.蒸馏 B.渗析 C.分液 D.萃取