题目内容
【题目】碘在科研与生活中有重要作用,某兴趣小组用0.50mol/L KI、0.2%淀粉溶液、0.10molL﹣1K2S2O8、0.20molL﹣1Na2S2O3等试剂,探究反应条件对化学反应速率的影响.
已知:S2O82﹣+2I﹣=2SO42﹣+I2(慢) I2+2S2O32﹣=2I﹣+S4O62﹣ (快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的_________耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,Na2S2O3与K2S2O8初始的体积v(Na2S2O3)与v(K2S2O8)量需满足的关系为:v(Na2S2O3)______v(K2S2O8)(填“>”,“<”,“=”),出现蓝色之前,I-在反应中起到的作用是_________。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验序号 | 体积V/ml | 出现蓝色的时间t/s | ||||
K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | ||
① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 | 10 |
② | 5.0 | V1 | 4.0 | 4.0 | 2.0 | 20 |
③ | 10.0 | V2 | 2.0 | 4.0 | 2.0 | 20 |
④ | 10.0 | V3 | 4.0 | 2.0 | 2.0 | 5 |
①表中V1________,V2_______,V3=______ .
②用K2S2O8表示实验序号①、②、④的速率分别为_____mol·L-1·s-1.
③根据实验结构,以下说法正确的有_____
A.该反应的速率与K2S2O8的浓度成正相关
B.该反应的速率与KI的浓度成正相关
C.该反应的速率与Na2S2O3的浓度成正相关
D.多步反应的速率由慢速反应速率决定
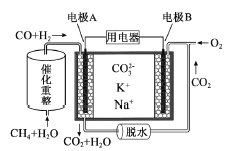
(3)已知某条件下,浓度c(S2O82﹣)随反应时间t的变化曲线如图,若保持其它条件不变,图中,分别画出降低反应温度和加入催化剂时c(S2O82﹣)随反应时间t的变化曲线示意图(进行相应的标注)_____.
【答案】 S2O32- < 催化剂 5.0 2.0 2 0.002、0.001、0.002 ACD 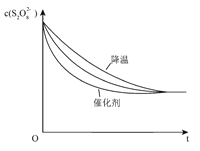
【解析】(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,先发生S2O82-+2I-═2SO42-+I2(慢),后发生I2+2S2O32-═S4O62-+2I-(快),当S2O32-耗尽后,碘才能与淀粉作用显示蓝色,根据I2+2S2O32-═S4O62-+2I-(快)方程式知,I2与S2O32-的物质的量的关系为1:2,即1mol碘需2molS2O32-,根据方程式S2O82-+2I-═2SO42-+I2知,生成1mol碘需为1molS2O82-,即n(S2O32-):n(S2O82-)=2:1,浓度之比也是2:1,为确保能观察到蓝色,碘需有剩余,即V(S2O2—3) <V(S2O2—8),I-在反应中起催化作用,故答案为:Na2S2O3;<;
(2)该实验的目的是探究反应物浓度对化学反应速率的影响,为保证K2S2O8溶液、KI溶液、Na2S2O3溶液浓度改变,而其他的条件不变才能达到实验目的,所以在实验各中溶液体积必须保持为20mL,所以①表中V1=5.0,V2=2.0,V3==2.0;
②通过K2S2O8——2Na2S2O3,但Na2S2O3浓度是K2S2O8浓度的2倍,Na2S2O3浓度的变化量等于K2S2O8浓度变化量,总体积为20mL,可分别求出①、②、④的速率分别为0.002 mol·L-1·s-1.、0.001 mol·L-1·s-1.、0.002 mol·L-1·s-1;③由以上对比实验分析出,该反应的速率与K2S2O8的浓度成正相关、与KI的浓度成正相关、多步反应的速率由慢速反应速率决定。
(3)保持其它条件不变,降低温度,反应速率降低,到达液颜色将由无色变成为蓝色的时间变长,而使用催化剂,能加快化学反应速率,所以到达液颜色将由无色变成为蓝色的时间变短,故答案为: .
.

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案