题目内容
【题目】同温同压下,下列各组热化学方程式中,△H1<△H2是( )
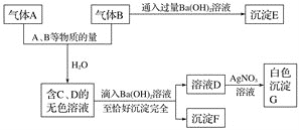
A. C(s)+![]() O2(g)=CO(g);△H1C(s)+O2(g)=CO2(g);△H2
O2(g)=CO(g);△H1C(s)+O2(g)=CO2(g);△H2
B. ![]() H2(g)+
H2(g)+![]() Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2HCl(g);△H2
Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2HCl(g);△H2
C. 2H2(g)+O2(g)=2H2O(g);△H1 2H2(g)+O2(g)=2H2O(l);△H2
D. S(g)+O2(g)=SO2(g);△H1 S(s)+O2(g)=SO2(g); △H2
【答案】D
【解析】
放热反应的ΔH为负值,反应放出的热量越多,其值越小。
A、前一个反应不完全燃烧,而后者完全燃烧,故ΔH1>ΔH2,也不符合;
B、热化学方程式的化学计量数改变后,ΔH也随之改变相同的倍数,故B项中ΔH1>ΔH2,,不符合;
C、由于H2O(g)液化为H2O(l),需放热,故C项中ΔH1>ΔH2,不符合;
D、由固态S转变为气态S需吸收热量,故A项中ΔH1<ΔH2,符合;
答案选D。

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目