题目内容
【题目】肼(N2H4)又称联氨,常用作火箭推进器的燃料。已知:
①N2(g)+O2(g)=2NO(g) ΔH1=+182kJ·mol-1;
②2NO(g) +O2(g)=2NO2(g) ΔH2=-114.3kJ·mol-1;
③2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ΔH2=-1135.7kJ·mol-1。
下列说法正确的是( )
A.N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH1=-1068kJ·mol-1
B.用铂作电极,以KOH溶液为电解液的肼![]() 空气燃料电池,放电时的负极反应为N2H4-4e-+4OH-=N2+4H2O
空气燃料电池,放电时的负极反应为N2H4-4e-+4OH-=N2+4H2O
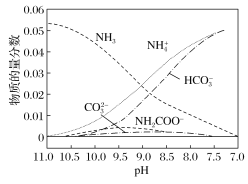
C.肼与氨类似,溶于水显碱性,可表示为N2H4+H2O=N2H5++OH-
D.某密闭容器中存在:2NO2(g)![]() N2O4(g),加压
N2O4(g),加压![]() 缩小体积
缩小体积![]() 后颜色先变深后变浅,不能用勒夏特列原理解释
后颜色先变深后变浅,不能用勒夏特列原理解释
【答案】B
【解析】
A.①N2(g)+O2(g)=2NO(g) ΔH1=+182kJ·mol-1;②2NO(g) +O2(g)=2NO2(g) ΔH2=-114.3kJ·mol-1;③2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ΔH2=-1135.7kJ·mol-1,根据盖斯定律,将![]() 得:N2H4(g)+O2(g)=N2(g)+2H2O(g)ΔH1=-534kJ·mol-1,故A错误;
得:N2H4(g)+O2(g)=N2(g)+2H2O(g)ΔH1=-534kJ·mol-1,故A错误;
B.该燃料电池中,负极上肼失电子发生氧化反应,电极反应式为N2H4-4e-+4OH-=N2+4H2O,故B正确;
C.肼是与氨类似的弱碱,它易溶于水,N2H4H2O存在电离平衡,电离出N2H5+、OH-,电离方程式为N2H4+H2ON2H5++OH-,故C错误;
D.加压时容器体积减小,二氧化氮浓度增大,气体颜色加深,平衡正向移动,气体颜色又变浅,能用平衡移动原理解释,故D错误;
故选B。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案