题目内容
15.下列各组物质全部是弱电解质的是( )| A. | H2SiO3、H2S、CO2 | B. | H2O、NH3•H2O、HClO | ||
| C. | H2SO3、Ba(OH)2、BaSO4 | D. | Cu(OH)2CH3COOH、C2H5OH、CH3COONa |
分析 电解质的强弱是根据电离程度划分的,在水溶液里或熔融状态下完全电离是电解质是强电解质,部分电离是电解质是弱电解质,强酸、强碱和大部分的盐属于强电解质.
解答 解:A.CO2溶于水虽然能导电,是由于二氧化碳与水反应生成的碳酸导电,不是二氧化碳自身电离,二氧化碳不是电解质,是非电解质,故A错误;
B.H2O、NH3•H2O、HClO在水溶液中部分电离,属于弱电解质,故B正确;
C.Ba(OH)2是强碱,BaSO4是盐,均全部电离,属于强电解质,故C错误;
D.C2H5OH不能导电,属于非电解质,故D错误,
故选B.
点评 本题考查了强弱电解质的判断,明确电解质的强弱是根据电离程度划分的,注意不能根据电解质溶液的导电性强弱划分强弱电解质,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.观察是研究物质性质一种基本方法.某同学将一小块金属钠露置空气中,观察到如下现象:银白色$\stackrel{①}{→}$变灰暗$\stackrel{②}{→}$变白色$\stackrel{③}{→}$出现液滴$\stackrel{④}{→}$白色固体,下列说法正确的是( )
| A. | ①是化合反应 | |
| B. | ②变白色是因为生成了碳酸钠 | |
| C. | ③是碳酸钠吸收空气中的水蒸气形成了溶液 | |
| D. | ④只发生物理变化 |
6.设NA是阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 0.1mo1•L-1MgCl2溶液中含C1一数为0.2 NA | |
| B. | 标准状况下,22.4L的CCl4中含CCl4分子数为NA | |
| C. | 0.1molNa2O2与足量的CO2完全反应转移电子数目为0.1NA | |
| D. | 10mL5mol•L-1(NH4)2CO3溶液中含有N原子数目小于0.1 NA |
3.下列有关电化学装置完全正确的是( )
| A. |  铜的冶炼 | B. | 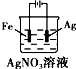 铁上镀银 | C. |  防止Fe被腐蚀 | D. |  构成铜锌原电池 |
10.若NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 等物质的量的N2与O2中的所含分子数均为NA | |
| B. | 标准状况下,5.6L CCl4含有的分子数为0.25NA | |
| C. | 常温常压下,22gCO2含有的原子数为1.5NA | |
| D. | 1mol/L NaOH溶液中含有的Na+的数目为NA |
20.下列有关安全问题的叙述不正确的是( )
| A. | 工业制取硝酸时尾气用氢氧化钠溶液吸收 | |
| B. | 氯气泄露时,应用蘸有肥皂水的湿毛巾捂住口鼻到安全区域 | |
| C. | 家中做卫生保洁时,严禁漂白粉与浓盐酸混合使用,否则会产生有毒气体 | |
| D. | 家中发生天然气泄露时,应立即使用室内电话报警 |
 已知:溴苯的熔点为?30.8℃,沸点156℃.实验室用苯和液溴制取溴苯的装置如图:
已知:溴苯的熔点为?30.8℃,沸点156℃.实验室用苯和液溴制取溴苯的装置如图: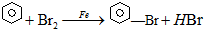 .;
.;


