题目内容
短周期元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列说法不正确的是
| A.X是钠元素 |
| B.离子半径X+>Z2- |
| C.同族元素中Z的氢化物稳定性最强 |
| D.同周期元素中Y的非金属性最强 |
B
解析试题分析:X、Y在同一周期,只可能为二、三周期。X+与Z2-具有相同的核外电子层结构,说明X比Z多一个电子层,所以X、Y为第三周期元素,Z为第二周期元素,X为Na,Y为Cl、Z为O。根据元素周期律分析,电子层数相同,原子序数越大,离子半径越小,B错误。
考点:考查元素推断、元素周期律。

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案
相关题目
X、Y、Z、W四种元素在元素周期表中的相对位置如下图所示,其中X、W的质子数之和为21,由此可知
| | X | | Y |
| Z | | W | |
A.X位于元素周期表中第2周期、第ⅤA族
B.Y的氢化物(H2Y)不稳定,100℃以上即可分解
C.Z的最高价氧化物的水化物是一种强碱
D.W的非金属性比Y的非金属性弱
短周期元素中,原子基态时具有1个未成对电子的元素共有多少种( )
| A.5 | B.6 | C.7 | D.8 |
短周期元素X,Y,Z,W在周期表中相对位置如下图所示,Y元素在地壳中的含量最高。下列说法正确的是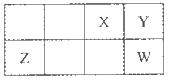
| A.原子半径;Z<Y<W |
| B.最简单气态氢化物的热稳定性:Y<W |
| C.含X的化合物形成的溶液一定呈酸性 |
| D.X的最简单阴离子和Z的最简单阳离子核外电子数相同 |
下列表示式错误的是( )。
A.Na+的轨道表示式 |
B.Na+的结构示意图: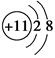 |
| C.Na的电子排布式:1s22s22p63s1 |
| D.Na的简化电子排布式:[Ne]3s1 |
下列电子排布式中,原子处于激发态的是( )。
| A.1s22s22p5 |
| B.1s22s22p43s2 |
| C.1s22s22p63s23p63d54s1 |
| D.1s22s22p63s23p63d34s2 |
下面关于多电子原子核外电子的运动规律的叙述正确的是( )。
| A.核外电子是分层运动的 |
| B.所有电子在同一区域里运动 |
| C.能量高的电子在离核近的区域运动 |
| D.不同能量的电子在核外运动占有的区域形状可能不同 |
自从1803年英国化学家、物理学家道尔顿提出了原子假说,人类对原子结构的认识就不断深入、发展,并通过实验事实不断地完善对原子结构的认识。下列关于原子结构模型的说法中,正确的是( )。
| A.道尔顿的原子结构模型将原子看作实心球,故不能解释任何问题 |
| B.汤姆逊“葡萄干布丁”原子结构模型成功地解释了原子中的正负粒子是可以稳定共存的 |
| C.卢瑟福核式原子结构模型指出了原子核和核外电子的质量关系、电性关系及占有体积的关系 |
| D.玻尔电子分层排布原子结构模型引入了量子化的概念,能够成功解释所有的原子光谱 |
X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如右图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )。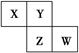
| A.原子半径:W>Z>Y>X |
| B.最高价氧化物对应水化物的酸性W比Z弱 |
| C.Y的气态氢化物的稳定性较Z的弱 |
| D.四种元素的单质中,Z的熔、沸点最高 |