题目内容
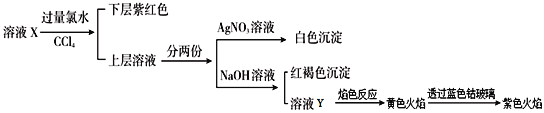
【题目】Fe3+与CN-、F-、有机分子等形成的化合物具有广泛的应用。
(1)Fe3+基态核外电子排布式为________。
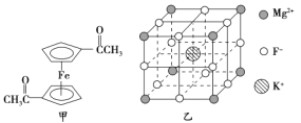
(2)乙酰基二茂铁是常用汽油抗震剂,其结构如图甲所示。此物质中碳原子的杂化方式是__________。
(3)C、N、O原子的第一电离能由大到小的顺序是___________________________。
(4)配合物K3Fe(CN)6可用于电子传感器的制作。与配体互为等电子体的一种分子的化学式为________________。已知(CN)2是直线形分子,并具有对称性,则(CN)2中π键和σ键的个数比为__________________。
(5)F-不仅可与Fe3+形成3-,还可以与Mg2+、K+形成一种立方晶系的离子晶体,此晶体应用于激光领域,其结构如图乙所示,则该晶体的化学式为__________________________。
【答案】 1s22s22p63s23p63d5(或3d5) sp3、sp2 N>O>C CO(或N2) 4∶3 KMgF3
【解析】(1)Fe的原子序数为26,Fe3+的基态核外电子排布式为1s22s22p63s23p63d5(或3d5)。
(2)根据图中乙酰基二茂铁的结构可知,碳原子的杂化方式有两种。其中形成碳氧双键的碳原子和五元环上的碳原子杂化方式是sp2杂化,而-CH3上的碳原子杂化方式是sp3杂化。
(3)根据元素周期律,可知同周期元素原子第一电离能随着原子序数的增加逐渐增大,由于原子轨道上电子处于全满、半满和全空时较稳定,所以第ⅡA、ⅢA族以及第ⅤA、ⅥA主族存在反常,即同周期元素第ⅡA族的第一电离能大于第ⅢA族的第一电离能,第ⅤA族的第一电离能大于第ⅥA族的第一电离能,因此![]() 、
、![]() 、
、![]() 原子的第一电离能由大到小的顺序是N>O>C。
原子的第一电离能由大到小的顺序是N>O>C。
(4)配合物K3Fe(CN)6的配体是CN-,有14个电子,因此与其互为等电子体的分子有两种:CO或N2;(CN)2是直线型分子且具有对称性,可以判断碳氮之间形成三键,碳碳之间为单键连接,其结构式为N≡C-C≡N,因此![]() 键有4个,
键有4个,![]() 键有3个,个数比为
键有3个,个数比为![]() 。
。
(5)由晶胞结构图可知:K+位于体心,F-位于棱上,Mg2+位于顶点,因此每个晶胞中有1个K+、1/4×12=3个F-,1/8×8=1个Mg2+,则该晶体的化学式为KMgF3。
【题型】综合题
【结束】
12
【题目】某树脂的合成线路如下:
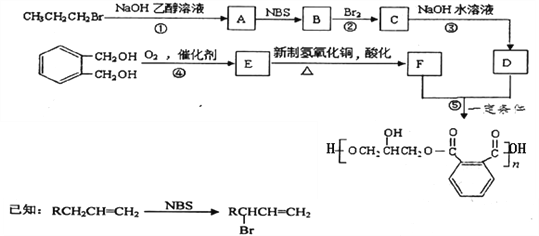
(1)B中含有的官能团的名称是________________________。
(2)反应①、③的有机反应类型分别是________________、____________________。
(3)检验CH3CH2CH2Br中的溴原子时,所加试剂的顺序依次是_______________。
(4)下列说法正确的是__________(填字母编号)。
a.1 mol E与足量的银氨溶液反应能生成2mol Ag
b.可以用NaHCO3鉴别E和F
c.B分子存在顺反异构
(5)写出反应⑤的化学方程式______________________________________________。
(6)![]() 的同分异构体中同时符合下列条件的芳香族化合物共有______种,其中苯环上一氯代物有两种的结构简式为_______________________。
的同分异构体中同时符合下列条件的芳香族化合物共有______种,其中苯环上一氯代物有两种的结构简式为_______________________。
a.能发生消去反应 b.能与过量浓溴水反应生成白色沉淀
【答案】 碳碳双键、溴原子 消去反应 取代反应(或水解反应) 过量氢氧化钠溶液、稀硝酸、硝酸银溶液 b 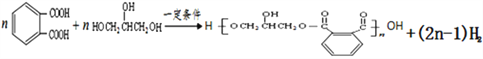 6
6 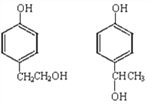
【解析】本题考查有机物的结构、性质、转化、反应类型、化学方程式和同分异构体的书写的知识。CH3CH2CH2Br与NaOH的乙醇溶液共热,发生消去反应产生A为丙烯:CH2=CH-CH3;CH2=CH-CH3与NBS发生取代反应产生B为:CH2=CHCH2Br;CH2=CHCH2Br与Br2发生加成反应,生成C为BrCH2CHBrCH2Br,BrCH2CHBrCH2Br在碱性条件下,在加热时水解,发生取代反应生成D为HOCH2CH(OH)CH2OH,根据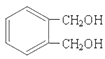 →E→F→
→E→F→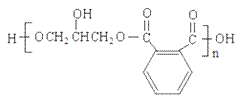 ,结合反应条件可知,E是
,结合反应条件可知,E是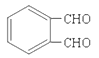 ;F是
;F是![]() 。D与F发生缩聚反应产生高聚物
。D与F发生缩聚反应产生高聚物 。
。
(1)B是CH2=CHCH2Br,则其中含有的官能团的名称是碳碳双键、溴原子。
(2) 反应①是CH3CH2CH2Br变为CH2=CH-CH3,反应类型是消去反应;反应③是BrCH2CHBrCH2Br变为HOCH2CH(OH)CH2OH,有机反应类型是取代反应(或水解反应)。
(3)检验CH3CH2CH2Br中的溴原子时,要先利用卤代烃可以在碱性条件下,在加热时发生取代反应,先加入NaOH的水溶液并加热;然后再加入硝酸酸化,除去其中含有的过量的NaOH溶液,最后加入AgNO3溶液,根据AgBr是难溶性的淡黄色的沉淀检验,所加试剂的顺序依次是过量氢氧化钠溶液、稀硝酸、硝酸银溶液。
(4)a. 由于在E分子中含有2个醛基,所以1 mol E与足量的银氨溶液反应能生成4mol Ag,错误;b.E是邻苯二甲醛,F是邻苯二甲酸,前者不能与NaHCO3发生反应,而后者反应产生产生气体,所以可以利用NaHCO3鉴别二者;c.B分子存在在一个不饱和的碳原子连接2个H原子,所以不存在顺反异构,错误;
(5)反应⑤的化学方程式是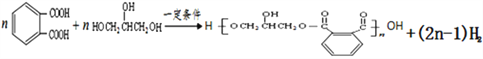 ;
;
(6) 同时符合条件a.能发生消去反应;b.能与过量浓溴水反应生成白色沉淀的同分异构体有
同时符合条件a.能发生消去反应;b.能与过量浓溴水反应生成白色沉淀的同分异构体有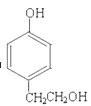 、
、 以及这两种物质的基团在邻位和间位的化合物,共有6种。其中苯环上一氯代物有两种的结构简式为
以及这两种物质的基团在邻位和间位的化合物,共有6种。其中苯环上一氯代物有两种的结构简式为 、
、 。
。

 阅读快车系列答案
阅读快车系列答案