题目内容
8.在实验室里可用如图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.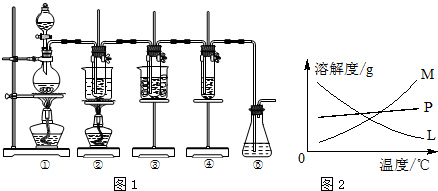
图中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过分液漏斗(填写仪器名称)向烧瓶中加入适量的浓盐酸.实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有B(填写下列编号字母)的净化装置.
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是:碱溶液(或反应物)的浓度不同,反应温度不同.
反应完毕经冷却后,②的试管中有大量晶体析出.右图中符合该晶体溶解度曲线的是M(填写编号字母).
(3)本实验中制取氯酸钾的离子方程式是3Cl2+6OH-=ClO3-+5Cl-+3H2O.
分析 (1)依据图中仪器特点结合分液漏斗的作用解答;
氯化氢易挥发,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大;
(2)温度与浓度不同,影响发生的氧化还原反应;冷却后,②的试管中有大量晶体析出,则其溶解度受温度影响较大,且随温度升高而增大;
(3)氯气与氢氧化钠在加热条件下反应生成氯酸钾和氯化钾和水.
解答 解:(1)制取氯气时,用分液漏斗盛放并向烧瓶中加入盐酸;
因为氯化氢易挥发,所以制取的氯气中含有氯化氢,可用饱和食盐水除去氯气中的氯化氢;
故答案为:分液漏斗;B;
(2)制取氯酸钾和次氯酸钠的条件有两个不同点:①制取温度不同;②制取时碱的浓度也不同;
冷却后,②的试管中有大量晶体析出,则其溶解度受温度影响较大,且随温度升高而增大,则曲线M符合;
故答案为:制取温度不同;制取时碱的浓度也不同; M;
(3)氯气与氢氧化钠在加热条件下反应生成氯酸钾和氯化钾和水,离子方程式:3Cl2+6OH-=ClO3-+5Cl-+3H2O;
故答案为:3Cl2+6OH-=ClO3-+5Cl-+3H2O.
点评 本题考查实验方案的设计,熟悉氯气的制取原理及物质的性质是解答本题的关键,注意反应条件对发生反应的影响,题目难度不大.

练习册系列答案
相关题目
18. 有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中Cl-与SO42-之比为( )
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中Cl-与SO42-之比为( )
 有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中Cl-与SO42-之比为( )
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中Cl-与SO42-之比为( )| A. | 2:3 | B. | 1:3 | C. | 3:2 | D. | 2:1 |
19.一定温度下在容积恒定的密闭容器中,进行如下可逆反应:A(s)+2B(g)?C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是( )
①混合气体的密度不再变化时
②容器内气体的压强不再变化时
③混合气体的总物质的量不再变化时
④B的物质的量浓度不再变化时
⑤混合气体的平均相对分子质量不再改变的状态
⑥当V正(B)=2V逆(C)
①混合气体的密度不再变化时
②容器内气体的压强不再变化时
③混合气体的总物质的量不再变化时
④B的物质的量浓度不再变化时
⑤混合气体的平均相对分子质量不再改变的状态
⑥当V正(B)=2V逆(C)
| A. | ①④⑤⑥ | B. | ②③⑥ | C. | ②④⑤⑥ | D. | 只有④ |
16.有Al2(SO4)3和Na2SO4的混合溶液VL,将它均分成两份.一份滴加氨水,使Al3+离子完全沉淀;另一份滴加BaCl2溶液,使SO42-离子完全沉淀.反应中消耗a mol NH3•H2O、b mol BaCl2.据此得知原混合溶液中的c(Na+)(mol/L)为( )
| A. | $\frac{4b-2a}{V}$ | B. | (2b-2a)/V | C. | (2b-a)/V | D. | (b-2a)/V |
3.将3.48g四氧化三铁完全溶解在100mL 1mol•L-1 的硫酸中,然后加入K2Cr2O7溶液25mL,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O72-全部转化为Cr3+,则K2Cr2O7溶液的物质的量浓度是( )
| A. | 0.05mol•L-1 | B. | 0.1mol•L-1 | C. | 0.2mol•L-1 | D. | 0.3mol•L-1 |
20.对复杂的有机物结构可用“键线式”表示.如苯丙烯酸丙烯酯: 可简化为:
可简化为: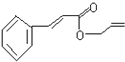 杀虫剂“阿乐丹”的结构表示为:
杀虫剂“阿乐丹”的结构表示为: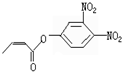 ,它在稀酸作用下能发生水解反应生成两种有机物.下列关于这两种有机物的共同性质叙述不正确的是( )
,它在稀酸作用下能发生水解反应生成两种有机物.下列关于这两种有机物的共同性质叙述不正确的是( )
 可简化为:
可简化为: 杀虫剂“阿乐丹”的结构表示为:
杀虫剂“阿乐丹”的结构表示为: ,它在稀酸作用下能发生水解反应生成两种有机物.下列关于这两种有机物的共同性质叙述不正确的是( )
,它在稀酸作用下能发生水解反应生成两种有机物.下列关于这两种有机物的共同性质叙述不正确的是( )| A. | 遇FeCl3溶液均显紫色 | B. | 均能发生氧化反应 | ||
| C. | 均能与溴水发生反应 | D. | 均能与NaOH溶液发生反应 |
17.除去下列物质中的少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 溴苯(溴) | 氢氧化钠溶液 | 过滤 |
| B | 苯(甲苯) | 酸性高锰酸钾溶液 | 分液 |
| C | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
| D | 溴乙烷(乙醇) | 蒸馏水 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
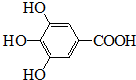 300多年前,著名化学家波义耳发现了铁盐与没食子酸的显色反应,并由此发明了蓝黑墨水.没食子酸的结构式为:
300多年前,著名化学家波义耳发现了铁盐与没食子酸的显色反应,并由此发明了蓝黑墨水.没食子酸的结构式为: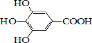 +4NaOH→
+4NaOH→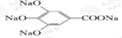 +4H2O.
+4H2O.