题目内容
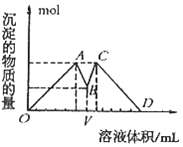
【题目】如图所示是向MgCl2、AlCl3混合液中依次加入M和N时生成沉淀的物质的量与加入的M和N的体积关系图(M、N各表示盐酸或氢氧化钠溶液中的一种),以下结论正确的是( )
A.混合溶液中c(AlCl3):c(MgCl2)=1:1
B.混合溶液中c(AlCl3):c(MgCl2)=3:1
C.V之前加盐酸,V之后加NaOH溶液
D.这种盐酸与NaOH溶液中溶质的物质的量浓度为2:1
【答案】A
【解析】
由图象可知A→B发生Al(OH)3+OH﹣═AlO2﹣+2H2O,设消耗氢氧化钠nmol,n(Al(OH)3)=n(AlCl3)=nmol,OA消耗氢氧化钠5nmol,分别发生
MgCl2+2NaOH=Mg(OH)2↓+2NaCl AlCl3+3NaOH=Al(OH)3↓+3NaCl
nmol 2nmol nmol 3nmol
可知n(MgCl2)=(5nmol﹣1×3nmol) ÷2=2nmol,则c(AlCl3):c(MgCl2)=nmol :nmol=1:1,B点时溶液成分为NaAlO2,之后继续加入N,沉淀质量逐渐增大,应加入盐酸,B→C发生NaAlO2+HCl+H2O=Al(OH)3↓+NaCl,继续加入盐酸沉淀逐渐溶解,生成氯化镁和氯化铝,B→C发生NaAlO2 +HCl+H2O=Al(OH)3↓+NaCl,由横坐标可知消耗盐酸和氢氧化钠的体积相同,则二者物质的量浓度相同,综上分析可知选项A,故答案为A。

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目