题目内容
20.在Al(NO3)3和NaHSO4的混合溶液,能够大量共存的粒子组是( )| A. | Ba2+、OH-、Mg2+、Cl- | B. | Fe2+、SO32-、Cu2+、AlO2- | ||
| C. | HCO3-、I-、Cl-、Cu2+ | D. | Fe3+、Cu2+、Cl-、H+、 |
分析 在Al(NO3)3和NaHSO4的混合溶液中存在铝离子、氢离子和硫酸根离子,
A.氢氧根离子与镁离子、氢离子反应,钡离子与硫酸根离子反应;
B.氢离子与亚硫酸根离子、偏铝酸根离子反应;亚铁离子、铜离子与亚硫酸根离子、偏铝酸根离子反应;
C.碳酸氢根离子与铜离子、铝离子发生双水解反应,氢离子与碳酸氢根离子反应;
D.四种离子之间不反应,都不与硫酸氢钠和硝酸铝反应.
解答 解:在Al(NO3)3和NaHSO4的混合溶液中含有铝离子、氢离子和硫酸根离子,
A.OH-、Mg2+之间反应氢氧化镁沉淀,OH-、H+之间反应生成水,Ba2+、SO42-之间反应生成硫酸钡沉淀,在溶液中不能大量共存,故A错误;
B.Fe2+、H+、Cu2+与SO32-、AlO2-之间反应,在溶液中不能大量共存,故B错误;
C.HCO3-与Al3+、Cu2+之间发生双水解反应,HCO3-、H+之间反应,在溶液中不能大量共存,故C错误;
D.Al3+、Cu2+、Cl-、H+、之间不反应,都不与Al(NO3)3和NaHSO4的混合溶液反应,在溶液中不能大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
11.下列化学用语的表示错误的是( )
| A. | 氯离子的结构示意图: | |
| B. | 甲基的电子式: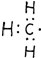 | |
| C. | Na+的电子排布图: | |
| D. | 硫离子的核外电子排布式:1S22S22P63S23P6 |
8.向含有Mn2+的酸性溶液中滴加二硫酸钾(K2S2O8)溶液,发生如下反应(未配平,不考虑滴加后溶液体积变化):Mn2++S2O82-+H2O→MnO${\;}_{4}^{-}$+SO42-+H+,下列说法正确的是( )
| A. | 反应后溶液的pH降低 | |
| B. | 该反应中起氧化作用的是Mn2+ | |
| C. | 有1mol还原剂参加反应时,转移4mol电子 | |
| D. | 检验Mn2+存在的实验现象是溶液紫红色消失 |
15. 如图(Ⅰ)表示反应:mA(g)+nB(g)?pC(g)+qD(g);△H.在不同温度下经过一定时间混合气体体系中C的百分含量与温度T的关系.图(Ⅱ)表示在一定条件下达到平衡后,t时刻改变压强,重新建立平衡的反应过程.由此可判断该反应中( )
如图(Ⅰ)表示反应:mA(g)+nB(g)?pC(g)+qD(g);△H.在不同温度下经过一定时间混合气体体系中C的百分含量与温度T的关系.图(Ⅱ)表示在一定条件下达到平衡后,t时刻改变压强,重新建立平衡的反应过程.由此可判断该反应中( )
 如图(Ⅰ)表示反应:mA(g)+nB(g)?pC(g)+qD(g);△H.在不同温度下经过一定时间混合气体体系中C的百分含量与温度T的关系.图(Ⅱ)表示在一定条件下达到平衡后,t时刻改变压强,重新建立平衡的反应过程.由此可判断该反应中( )
如图(Ⅰ)表示反应:mA(g)+nB(g)?pC(g)+qD(g);△H.在不同温度下经过一定时间混合气体体系中C的百分含量与温度T的关系.图(Ⅱ)表示在一定条件下达到平衡后,t时刻改变压强,重新建立平衡的反应过程.由此可判断该反应中( )| A. | m+n>p+q,△H<0 | B. | m+n>p+q,△H>0 | C. | m+n<p+q,△H>0 | D. | m+n<p+q,△H<0 |
5.如图是三种稀酸对Fe-Cr合金的腐蚀性随Cr含量变化的实验结果,下列有关说法正确的是( )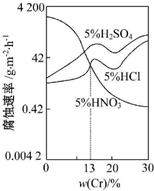

| A. | 稀硝酸对Fe-Cr合金的腐蚀性比稀硫酸和稀盐酸的弱 | |
| B. | 随着Cr含量增加,稀硝酸对Fe-Cr合金的腐蚀性减弱 | |
| C. | Cr含量大于13%时,因为三种酸中硫酸的氢离子浓度最大,所以对Fe-Cr合金的腐蚀性最强 | |
| D. | 稀硝酸和铁反应的化学方程式:Fe+6HNO3(稀)=Fe(NO3)3+3NO2↑+3H2O |
12.下列各组仪器中,能用酒精灯直接加热的一组是( )
| A. | 燃烧匙、集气瓶 | B. | 蒸发皿、试管 | C. | 坩埚、烧杯 | D. | 烧瓶、烧杯 |
9.下列说法不正确的是( )
| A. | 化学反应过程中吸收或释放的热量称为反应热 | |
| B. | 已知:2H2(g)+O2(g)═2H2O(l)△H1=-571.6 kJ•mol-1,是指每摩尔氢气完全燃烧放出的热量571.6 kJ | |
| C. | 醋酸与氢氧化钠溶液的中和反应是放热反应 | |
| D. | 热化学方程式中各物质前面的化学计量数可以是分数 |
10.选择环保的装修材料可以有效地减少居室污染.劣质胶合板释放出的主要污染物是( )
| A. | NO | B. | CO | C. | 甲醛 | D. | CO2 |