题目内容
【题目】将一定量的铜粉加入到0.5 L 0.3 mol·L-1 Fe2(SO4)3和0.1 mol·L-1 H2SO4的混合溶液中,铜粉完全溶解后,得到溶液X。下列说法正确的是( )
A.溶液X中Cu2+与Fe2+的物质的量之比为2∶1
B.向溶液X中加入足量铁粉,充分反应后,铁粉质量减少11.2 g
C.向溶液X中滴加KSCN溶液,未变红色,则加入铜粉质量为12.8 g
D.向溶液X中加入0.18 L 5 mol·L-1 NaOH溶液可使溶液中的金属离子完全沉淀
【答案】B
【解析】
0.5L0.3molL1Fe2(SO4)3和0.1molL1H2SO4的混合溶液中,n((Fe3+)=cV=0.5L×2×0.3 mol·L-1 =0.3mol,n((H+)=cV=0.5L×2×0.1 mol·L-1 =0.1mol,n(SO42)= ![]() n((Fe3+)+
n((Fe3+)+![]() n((H+)=0.5mol,发生Cu+2Fe3+═Cu2++2Fe2+,所得溶液中Fe3+、Cu2+的物质的量与铜粉的量有关。
n((H+)=0.5mol,发生Cu+2Fe3+═Cu2++2Fe2+,所得溶液中Fe3+、Cu2+的物质的量与铜粉的量有关。
A. 发生Cu+2Fe3+═Cu2++2Fe2+,所得溶液中Cu2+与Fe2+的物质的量之比为1:2,故A错误;
B.向溶液X中加入足量铁粉,因铁离子的氧化性强于铜,所以铁先与三价铁反应,后置换出铜,最后与酸反应,因铁足量,相当于铁和原来的铁离子、氢离子反应,与加入的铜的量的多少无关,0.5L0.3molL1Fe2(SO4)3和0.1molL1H2SO4的混合溶液中,n(Fe3+)=cV=0.3molL1×0.5L×2=0.3mol,n((H+)=0.1mol,所以,发生Fe+2Fe3+═3Fe2+,消耗n(Fe)=0.15mol,发生Fe+2H+=Fe2++H2↑,消耗n(Fe)=0.05mol,总共消耗n(Fe)=0.15mol+0.05mol=0.2mol,充分反应后,铁粉质量减少m=nM=0.2mol×56g/mol=11.2g,故B正确;
C.混合溶液中,n((Fe3+)=cV=0.3mol,发生Cu+2Fe3+═Cu2++2Fe2+,未变红色,则三价铁完全反应,消耗n(Cu)=0.15mol,m=nM=0.15mol×64g/mol=9.6g,故C错误;
D.铜完全溶解时,溶液中可能存在的Fe2+、Cu2+、H+三种离子,或铜完全溶解时,溶液中的Fe3+、Fe2+、Cu2+、H+四种离子,沉淀完全,溶质为硫酸钠(Na2SO4),n(SO42) =0.5mol,所以n(Na+)=1mol,需NaOH的物质的量为1mol,加入0.18L5molL1NaOH溶液,氢氧化钠量为0.18 L×5 molL1=0.9mol,则氢氧化钠的量不足,不能完全沉淀,故D错误;
答案选B。

【题目】影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1)设计实验方案来研究影响化学反应速率的因素。甲同学的实验报告如下表:
实验步骤 | 现象 | 结论 |
①分别取等体积的2 mol·L-1的硫酸于试管中 | 反应速率Mg>Fe,Cu不反应 | 金属的性质越活泼,反应速率越快 |
②____________ | 反应物浓度越大,反应速率越快 |
(1)甲同学表中实验步骤②为_________________________________________。
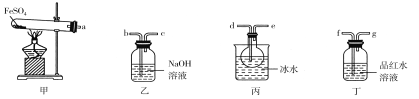
(2)甲同学的实验目的是_____________;要得出正确的实验结论,还需控制的实验条件是____________。乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验。

(3)乙同学在实验中应该测定的数据是___________________________________________________。
(4)乙同学完成该实验应选用的实验药品是________,该实验中不选用某浓度的硫酸,理由是___________。
实验二:已知 2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(5)针对上述实验现象,丙同学认为KMnO4与H2C2O4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是______________的影响。
(6)若用实验证明你的猜想,除高锰酸钾酸性溶液、草酸溶液外,还需要选择的试剂最合理的是________(填字母)。
A.硫酸钾 B.硫酸锰 C.二氯化锰 D.水