题目内容
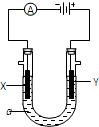 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X电极上的电极反应是
②Y电极上的电极反应
(2)若X和Y仍均为惰性电极,a为CuSO4溶液,则电解时的化学反应方程式为
(3)如果用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是
②Y电极的材料是
(说明:杂质发生的电极反应不必写出)
分析:(1)电解饱和氯化钠溶液时,由电源可知,X为阴极,Y为阳极,阳极上是氯离子离子失电子,阴极上是氢离子得电子;
(2)根据电解硫酸铜溶液电解电极反应的工作原理知识来回答;
(3)电解方法精炼粗铜,阳极材料是粗铜,阴极材料是精铜,电解质溶液必须是含有铜离子的盐溶液.
(2)根据电解硫酸铜溶液电解电极反应的工作原理知识来回答;
(3)电解方法精炼粗铜,阳极材料是粗铜,阴极材料是精铜,电解质溶液必须是含有铜离子的盐溶液.
解答:解:(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,X电极负极水的电离被破坏,氢氧根离子浓度增大,溶液呈红色,故答案为:2H++2e-=H2↑;溶液呈红色;
②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,检验氯气的方法是用湿润的淀粉碘化钾试纸检验生成的气体,气体能使试纸变蓝色,
故答案为:2Cl--2e-=Cl2↑;用湿润的淀粉碘化钾试纸检验生成的气体,气体能使试纸变蓝色;
(2)若X和Y仍均为惰性电极,a为CuSO4溶液,则电解时的总化学反应方程式为2CuSO4+2H2O
2Cu+O2↑+2H2SO4,通电一段时间后,向所得溶液中加入16gCuO粉末,物质的量=
=0.2mol,恰好恢复到电解前的浓度和pH,则生成的硫酸为0.2mol,反应的硫酸铜物质的量为0.2mol,转移电子0.4mol,
故答案为:2CuSO4+2H2O
2Cu+O2↑+2H2SO4;0.4mol;
(3)电解方法精炼粗铜,阳极材料是粗铜,阴极材料是精铜,电解质溶液必须是含有铜离子的盐溶液,可以是硫酸铜溶液,
①X电极是阴极,该电极材料应该是精铜,电极反应为:Cu2++2e-=Cu,故答案为:精铜;Cu2++2e-=Cu;
②Y电极是阳极,该电极材料是粗铜,电极反应为:Cu-2e-=Cu2+,故答案为:粗铜;Cu-2e-=Cu2+.
②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,检验氯气的方法是用湿润的淀粉碘化钾试纸检验生成的气体,气体能使试纸变蓝色,
故答案为:2Cl--2e-=Cl2↑;用湿润的淀粉碘化钾试纸检验生成的气体,气体能使试纸变蓝色;
(2)若X和Y仍均为惰性电极,a为CuSO4溶液,则电解时的总化学反应方程式为2CuSO4+2H2O
| ||
| 16g |
| 80g/mol |
故答案为:2CuSO4+2H2O
| ||
(3)电解方法精炼粗铜,阳极材料是粗铜,阴极材料是精铜,电解质溶液必须是含有铜离子的盐溶液,可以是硫酸铜溶液,
①X电极是阴极,该电极材料应该是精铜,电极反应为:Cu2++2e-=Cu,故答案为:精铜;Cu2++2e-=Cu;
②Y电极是阳极,该电极材料是粗铜,电极反应为:Cu-2e-=Cu2+,故答案为:粗铜;Cu-2e-=Cu2+.
点评:本题考查学生电解池的工作原理以及电解原理的应用知识,属于综合知识的考查,难度不大.

练习册系列答案
相关题目
 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
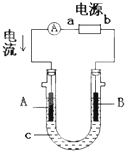 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题: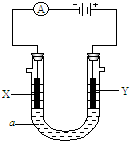 (I)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2.
(I)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2.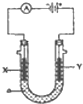 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连.