��Ŀ����
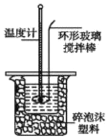
����Ŀ����ͼ��ʾ��������A�е�Ũ����μӵ�ʢ��MnO2����ƿ�У����Ⱥ��������������ͨ��װ��B��C��Ȼ����ͨ�����ȵ�ʯӢ������D�����������ۣ�����ش�

��1������A��������__________����ƿ�з�Ӧ�Ļ�ѧ����ʽ��_____________________��
��2��װ��B��ʢ����Һ����_______������ͨ��װ��B��Ŀ����___________________��
װ��C��ʢ�ŵ�Һ����_______������ͨ��װ��C��Ŀ����___________________��
��3��D�з�Ӧ�Ļ�ѧ����ʽ��_________________________________________________��
��4���ձ�E��ʢ�ŵ�Һ����__________����Ӧ�����ӷ���ʽ��__________��
���𰸡� ��Һ©�� 4HCl(Ũ)��MnO2![]() MnCl2��Cl2����2H2O ����NaCl��Һ ���������л��е�����HCl Ũ���� ����ˮ�������������� 2Fe��3Cl2
MnCl2��Cl2����2H2O ����NaCl��Һ ���������л��е�����HCl Ũ���� ����ˮ�������������� 2Fe��3Cl2![]() 2FeCl3 NaOH��Һ 2OH����Cl2��Cl����ClO����H2O
2FeCl3 NaOH��Һ 2OH����Cl2��Cl����ClO����H2O
����������1��װ����AΪ��Һ©������������ƿ�м���Ũ����Ͷ������̻���ȷ�Ӧ�����Ȼ��̡�������ˮ����Ӧ�Ļ�ѧ����ʽΪ��4HCl��Ũ��+MnO2![]() MnCl2+Cl2��+2H2O��
MnCl2+Cl2��+2H2O��
��2����Ӧ���ɵ������к����Ȼ����ˮ�����������壬�Ȼ��⼫������ˮ�������ڱ���ʳ��ˮ���ܽ��Լ�����ͨ������ʳ��ˮ��ȥ�Ȼ������壬ͨ��Ũ������Һ����ˮ������װ��B��ʢ��Һ���DZ���ʳ��ˮ������ͨ��װ��B��Ŀ�������������л��е�����HCl��װ��C��ʢ�ŵ�Һ����Ũ���ᣬ����ͨ��װ��C��Ŀ��������ˮ����������������
��3�����������ͨ��װ��D�������������������·�Ӧ�����Ȼ����ķ�Ӧ����Ӧ�Ļ�ѧ����ʽΪ��2Fe+3Cl2![]() 2FeCl3��
2FeCl3��
��4�������ж��������ŷŵ������У�װ��E������������Һ����������δ��Ӧ����������ֹ��Ⱦ����������������������Һ��Ӧ�����Ȼ��ơ��������ƺ�ˮ����Ӧ�����ӷ���ʽΪ��2OH-+Cl2=Cl-+ClO-+H2O��

 ȫ��������ϵ�д�
ȫ��������ϵ�д�����Ŀ��1Lij�����Һ�п��ܺ��е��������±���
���ܴ������е������� | H+��NH4+ ��Al3+��K+ |
���ܴ������е������� | Cl����Br����I����ClO����AlO2�� |
��1��������Һ����μ���NaOH��Һ���ʵ����ȣ�������������������ʵ�����n�������NaOH��Һ�������v���Ĺ�ϵ��ͼ��ʾ��
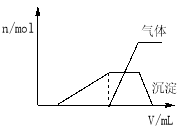
�������Һ��ȷ�����е������� ��
������ȷ���Ƿ��е��������� ��
��Ҫȷ������ڿɲ�������ʵ���� ��
���϶������ڵ��������� ��
��2������⣬����Һ�к��д�����Cl����Br����I��������1L�û����Һ��ͨ��һ������Cl2����Һ��Cl����Br����I�������ʵ�����ͨ��Cl2���������״�����Ĺ�ϵ���±���ʾ��������ش��������⣺
Cl2���������״���� | 2.8L | 5.6L | 11.2L |
n��Cl���� | 1.25mol | 1.5mol | 2mol |
n��Br���� | 1.5mol | 1.4mol | 0.9mol |
n��I���� | a mol | 0 | 0 |
����ͨ��Cl2�����Ϊ2.8Lʱ����Һ�з�����Ӧ�����ӷ���ʽΪ ��
��ԭ��Һ��Cl����Br����I�������ʵ���Ũ��֮��Ϊ ��
����Ŀ���������ʷ������ȷ������� ��
�� | �� | �� | ���������� | |
A | ���� | ���� | �ռ� | ������̼ |
B | �ռ� | ���� | ʳ�� | һ����̼ |
C | ������ | ���� | ʯ��ʯ | ˮ |
D | ���Լ� | ���� | �մ� | �������� |