��Ŀ����
����Ŀ��1Lij�����Һ�п��ܺ��е��������±���
���ܴ������е������� | H+��NH4+ ��Al3+��K+ |
���ܴ������е������� | Cl����Br����I����ClO����AlO2�� |
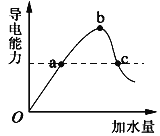
��1��������Һ����μ���NaOH��Һ���ʵ����ȣ�������������������ʵ�����n�������NaOH��Һ�������v���Ĺ�ϵ��ͼ��ʾ��
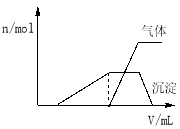
�������Һ��ȷ�����е������� ��
������ȷ���Ƿ��е��������� ��
��Ҫȷ������ڿɲ�������ʵ���� ��
���϶������ڵ��������� ��
��2������⣬����Һ�к��д�����Cl����Br����I��������1L�û����Һ��ͨ��һ������Cl2����Һ��Cl����Br����I�������ʵ�����ͨ��Cl2���������״�����Ĺ�ϵ���±���ʾ��������ش��������⣺
Cl2���������״���� | 2.8L | 5.6L | 11.2L |
n��Cl���� | 1.25mol | 1.5mol | 2mol |
n��Br���� | 1.5mol | 1.4mol | 0.9mol |
n��I���� | a mol | 0 | 0 |
����ͨ��Cl2�����Ϊ2.8Lʱ����Һ�з�����Ӧ�����ӷ���ʽΪ ��
��ԭ��Һ��Cl����Br����I�������ʵ���Ũ��֮��Ϊ ��
���𰸡���1����H+��NH4+��Al3+����K+������ɫ��Ӧ����ClO����AlO2��
��2����Cl2+2I���TI2+2Cl������10��15��4
��������
�����������1������ͼ��һ��ʼ�������ƶ���Һ��һ������H+����NaOH������ų������ƶ���Һ��һ������NH4+�����������ȫ��ʧ������Һ��ֻ����Al3+����������Mg2+��K+����ȷ������Ҫȷ��K+����ͨ����ɫ��Ӧȷ������Ϊ��Һ�к���H+������һ��������CO3 2-��AlO2-��������Һ��ȷ�����е��������У�H+��NH4+��Al3+��K+������ȷ��������Ϊ��K+���϶������ڵ��������У�CO3 2-��AlO2-��
��2����n��Cl2����2.8L��22.4L/mol��0.125mol��ͨ������������I-��Ӧ�����ɵ��ʵ⣬����ʽΪ��Cl2+2I-��I2+2Cl-��
��2.8Lʱ��n��Br-��=1.5mol����ԭ��Һ��n��Br-����1.5mol��������������n��Cl-����0.125��2��0.25mol����ԭ��Һ��n��Cl-����1.25��0.25��1mol��5.6Lʱ��n��Br-����1.5��1.4��0.1mol��n��I-����0.25��0.1��0.15����ԭ��Һ��n��I-����0.25+0.15��0.4mol����ԭ��Һ��Cl-��Br-��I-�����ʵ���Ũ��֮��Ϊ��1��1.5��0.4=10��15��4��

 ��У����ϵ�д�
��У����ϵ�д�