题目内容
9.下列说法错误的是( )| A. | 硝酸能溶解除金、铂外的大多数金属 | |
| B. | 汽车尾气中含有NO和CO | |
| C. | 浓氨水可检验氯气管道漏气 | |
| D. | 制取二氧化氮时,常用水吸收尾气 |
分析 A.依据硝酸具有强的氧化性解答;
B.依据汽车尾气成分解答;
C.浓氨水挥发出的氨气和氯气发生氧化还原反应生成氮气和氯化铵,反应现象冒白烟;
D.二氧化氮与水反应生成一氧化氮,不能用水吸收二氧化氮;
解答 解:A.硝酸具有强的氧化性,能够和大多数金属除去铂合金外,发生反应,故A正确;
B.汽车尾气中含有NO和CO,故B正确;
C.浓氨水挥发出的氨气和氯气发生氧化还原反应生成氮气和氯化铵,3Cl2+8NH3=N2+6NH4Cl,反应过程中现象是冒白烟,浓氨水可检验氯气管道漏气,故C正确;
D.二氧化氮与水反应生成一氧化氮,仍然污染空气,所以不能用水吸收,故D错误;
故选:D
点评 本题考查了元素化合物知识,熟悉硝酸的强的氧化性、二氧化氮、一氧化氮、氨水的性质是解题关键,题目难度不大.

练习册系列答案
 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
20.下列无色溶液中,离子可大量共存的是( )
| A. | Cu2+、K+、OH-、CO32- | B. | H+、Ba2+、SO32-、Br - | ||
| C. | K+、Na+、Cl-、MnO4- | D. | Ca2+、Na+、HCO3-、I- |
1.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1L 0.1 mol/L NaHCO3溶液中含有HCO3-数目为0.1NA | |
| B. | 常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA | |
| C. | 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA | |
| D. | 1 mol Fe与足量稀HNO3反应,转移电子数目为2NA |
14.下列反应的离子方程式中正确的是( )
| A. | Na2O2与水反应:Na2O2+2H20═2Na++2OH-+H2↑ | |
| B. | FeSO4溶液与H2O2溶液混合:Fe2++H2O2+2H+═Fe3++2H2O | |
| C. | 向Na2SiO3溶液中通人过量的SO2:SiO32-+SO2+H2O═Na2SiO3↓+SO32- | |
| D. | NH4HCO3稀溶液与过量的Ca(OH)2溶液混合:NH4++HC03-+Ca2++2OH-═CaCO3↓+NH3•H2O+H20 |
1.化学与生产、生活、环境关系密切,下列说法正确的是( )
| A. | 提倡使用太阳能、风能、天然气、地热能等新能源,以保护环境 | |
| B. | “玉兔号”的太阳能电池板主要由二氧化硅制成 | |
| C. | 为除去锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加盐酸溶解 | |
| D. | 碱性洗涤剂的去污能力比中性洗涤剂弱,是由于油脂在中性溶液中更易水解 |
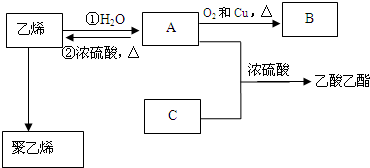
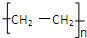 ,化合物C所含官能团的名称为羧基.
,化合物C所含官能团的名称为羧基.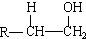 $→_{△}^{浓硫酸}$R-CH=CH2+H2O,写出反应②的反应方程式(标明反应条件):CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑.
$→_{△}^{浓硫酸}$R-CH=CH2+H2O,写出反应②的反应方程式(标明反应条件):CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑.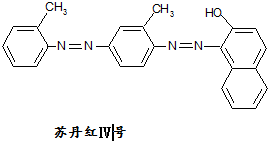 据2006年11月12 中央电视台每周质量报告报道,北京市场上销售的一部分标称是白洋淀特产的“红心鸭蛋”含偶氮染料“苏丹红Ⅳ号”,国际癌症研究机构将其列为三类致癌物.
据2006年11月12 中央电视台每周质量报告报道,北京市场上销售的一部分标称是白洋淀特产的“红心鸭蛋”含偶氮染料“苏丹红Ⅳ号”,国际癌症研究机构将其列为三类致癌物.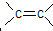 空间结构,且是不能旋转不然,双键就会被破坏,而单键是可以旋转的,则肯定共线的原子最多有12个.
空间结构,且是不能旋转不然,双键就会被破坏,而单键是可以旋转的,则肯定共线的原子最多有12个.