题目内容
常温时,反应2Fe3++Cu====2Fe2++Cu2+在水溶液中能发生。将22.4 g铜和三氧化二铁的混合粉末加入到浓度为1 mol·L-1的硫酸中,使之发生反应。(1)若固体恰好全部溶解,消耗硫酸的体积为V L,求V的取值范围。
(2)若硫酸溶液过量,反应后溶液的体积为1 L,测得此溶液中Fe2+浓度为0.1 mol·L-1,求原混合物中含铜多少克。
(1)0.3 L<V(H2SO4)<0.42 L
(2)3.2 g或14.4 g
解析:(1)固体恰好全部溶解,则n(Fe2O3)∶n(Cu)≥1∶1。如果22.4 g全部是Fe2O3,则V(H2SO4)=0.42 L;如果Fe2O3、Cu物质的量之比为1∶1,即各为0.1 mol,则V(H2SO4)=0.3 L。因为固体是Cu、Fe2O3的混合物,所以0.3 L<V(H2SO4)<0.42 L。
(2)Fe2+为0.1 mol,则反应的Fe2O3、Cu各为0.05 mol。若Fe2O3过量,则m(Cu)=0.05 mol×64 g·mol-1=3.2 g;若Cu过量,则m(Cu)=22.4 g-m(Fe2O3)=22.4 g-0.05 mol×160 g·mol-1=14.4 g。

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
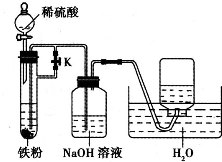 常温下,在没有氧气存在时,铁粉与水几乎不反应,但在高温下,铁粉能与水蒸气反应.
常温下,在没有氧气存在时,铁粉与水几乎不反应,但在高温下,铁粉能与水蒸气反应.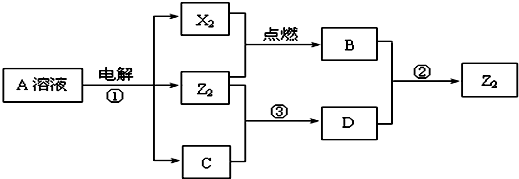
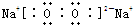
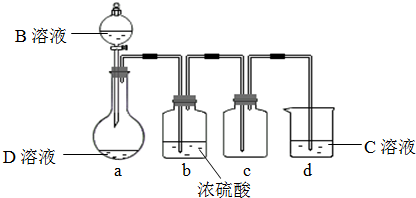
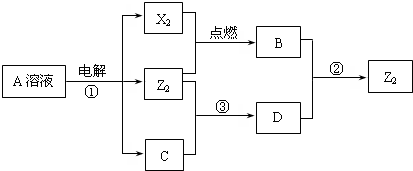
 2OH-+Cl2↑+H2↑
2OH-+Cl2↑+H2↑