��Ŀ����
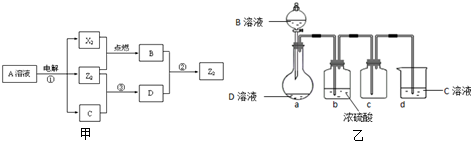
��֪��������֮����ʵ����ͼ����ʾ��ת����ϵ�����ֲ�������ȥ����
��1��Z2�Ľṹʽ��
��2����Ӧ�۵����ӷ���ʽ��
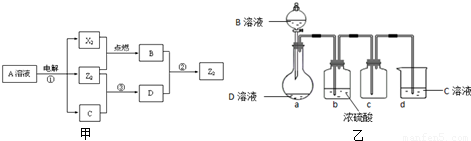
��3��D�Ǻܶ�Ư���к��е���Ч�ɷ֣���Щ��Ʒ���������飨�����л�������ᣩһ��ʹ�ã���ԭ������ڳ���ʱ�ܷ����뷴Ӧ�����Ƶķ�Ӧ��ijУ��ѧ����ʵ�������÷�Ӧ�ڵ�ԭ�����Ʊ������������Z2������װ����ͼ����ʾ���г̶ֹ�װ�õ���������ȥ����
I��д����Ӧ�ڵ����ӷ���ʽ
II������ʵ��װ�ò������ƣ��Ľ�������
������Z2 ͨ��FeBr2��Һ�з�����Ӧ�����ӷ���ʽ��

��1��Z2�Ľṹʽ��
Cl-Cl
Cl-Cl
����Ӧ�ٵ����ӷ���ʽ��2Cl-+2H2O
2OH-+Cl2��+H2��
| ||
2Cl-+2H2O
2OH-+Cl2��+H2��
��
| ||
��2����Ӧ�۵����ӷ���ʽ��
Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
����3��D�Ǻܶ�Ư���к��е���Ч�ɷ֣���Щ��Ʒ���������飨�����л�������ᣩһ��ʹ�ã���ԭ������ڳ���ʱ�ܷ����뷴Ӧ�����Ƶķ�Ӧ��ijУ��ѧ����ʵ�������÷�Ӧ�ڵ�ԭ�����Ʊ������������Z2������װ����ͼ����ʾ���г̶ֹ�װ�õ���������ȥ����
I��д����Ӧ�ڵ����ӷ���ʽ
ClO-+Cl-+2H+=Cl2��+H2O
ClO-+Cl-+2H+=Cl2��+H2O
��II������ʵ��װ�ò������ƣ��Ľ�������
��a��bװ��֮���һʢ�б���ʳ��ˮ��ϴ��ƿ����ȥHCl
��a��bװ��֮���һʢ�б���ʳ��ˮ��ϴ��ƿ����ȥHCl
��������Z2 ͨ��FeBr2��Һ�з�����Ӧ�����ӷ���ʽ��
2Fe2++4Br-+3Cl2=6Cl-+2Fe3++2Br2
2Fe2++4Br-+3Cl2=6Cl-+2Fe3++2Br2
����������1����2���ɷ�Ӧ��A��Һ�ڵ������������3�����ʣ�������������Ϊ˫ԭ�ӷ��ӣ�A����Ϊ�Ȼ�������Ӳ��ŵ磩��CΪ����Һ��BΪHCl��z2+���D����z2ΪCl2����Ϸ�Ӧ�ڿ�֪DΪ�������Σ���֤����ת����ϵ��
��3���������������£�Cl-��ClO-����Cl2��ˮ��
��Ӧ��ΪCl-+ClO-��Cl2������װ�����Ʊ������������Cl2��HCl�ӷ������Ʊ��������к���HCl��ˮ�����������ñ��͵��Ȼ�����Һ����HCl��������Ũ�������ɵô����������Cl2�������ж�����Ⱦ�������������������������Һ����β���е�������
����������ǿ�����ԣ���������������Ϊ�����ӣ�������������ΪBr2����������������Һ��Fe2+��Br-ȫ����������
��3���������������£�Cl-��ClO-����Cl2��ˮ��
��Ӧ��ΪCl-+ClO-��Cl2������װ�����Ʊ������������Cl2��HCl�ӷ������Ʊ��������к���HCl��ˮ�����������ñ��͵��Ȼ�����Һ����HCl��������Ũ�������ɵô����������Cl2�������ж�����Ⱦ�������������������������Һ����β���е�������
����������ǿ�����ԣ���������������Ϊ�����ӣ�������������ΪBr2����������������Һ��Fe2+��Br-ȫ����������
����⣺�ɷ�Ӧ��A��Һ�ڵ������������3�����ʣ�������������Ϊ˫ԭ�ӷ��ӣ�A����Ϊ�Ȼ�������Ӳ��ŵ磩��CΪ����Һ��BΪHCl��z2+���D����z2ΪCl2����Ϸ�Ӧ�ڿ�֪DΪ�������Σ�����ת����ϵ��
��1��������������֪��z2ΪCl2���ṹʽΪCl-Cl����Ӧ�ٵ���Ȼ�����Һ���ɼ��������������Ӧ���ӷ���ʽΪ��
2 Cl-+2H2O
2OH-+Cl2��+H2����
�ʴ�Ϊ��Cl-Cl��2 Cl-+2H2O
2OH-+Cl2��+H2����
��2��������Ӧ�����Ȼ���������Ρ�ˮ����Ӧ�۵����ӷ���ʽΪ��Cl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
��3���������������£�Cl-��ClO-����Cl2��ˮ����Ӧ���ӷ���ʽΪ��ClO-+Cl-+2H+=Cl2��+H2O��
�ʴ�Ϊ��ClO-+Cl-+2H+=Cl2��+H2O��
��Ӧ��ΪCl-+ClO-��Cl2������װ�����Ʊ������������Cl2��HCl�ӷ������Ʊ��������к���HCl��ˮ�����������ñ��͵��Ȼ�����Һ����HCl��������Ũ�������ɵô����������Cl2�������ж�����Ⱦ�������������������������Һ����β���е���������װ��ͼ��֪��ȱ������HCl��װ�ã�����a��bװ��֮���һʢ�б���ʳ��ˮ��ϴ��ƿ����ȥHCl��
�ʴ�Ϊ����a��bװ��֮���һʢ�б���ʳ��ˮ��ϴ��ƿ����ȥHCl��
����������ǿ�����ԣ���������������Ϊ�����ӣ�������������ΪBr2����������������Һ��Fe2+��Br-ȫ������������Ӧ���ӷ���ʽΪ��2 Fe2++4Br-+3Cl2=6Cl-+2 Fe3++2Br2��
�ʴ�Ϊ��2 Fe2++4Br-+3Cl2=6Cl-+2 Fe3++2Br2��
��1��������������֪��z2ΪCl2���ṹʽΪCl-Cl����Ӧ�ٵ���Ȼ�����Һ���ɼ��������������Ӧ���ӷ���ʽΪ��
2 Cl-+2H2O
| ||
�ʴ�Ϊ��Cl-Cl��2 Cl-+2H2O
| ||
��2��������Ӧ�����Ȼ���������Ρ�ˮ����Ӧ�۵����ӷ���ʽΪ��Cl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
��3���������������£�Cl-��ClO-����Cl2��ˮ����Ӧ���ӷ���ʽΪ��ClO-+Cl-+2H+=Cl2��+H2O��
�ʴ�Ϊ��ClO-+Cl-+2H+=Cl2��+H2O��
��Ӧ��ΪCl-+ClO-��Cl2������װ�����Ʊ������������Cl2��HCl�ӷ������Ʊ��������к���HCl��ˮ�����������ñ��͵��Ȼ�����Һ����HCl��������Ũ�������ɵô����������Cl2�������ж�����Ⱦ�������������������������Һ����β���е���������װ��ͼ��֪��ȱ������HCl��װ�ã�����a��bװ��֮���һʢ�б���ʳ��ˮ��ϴ��ƿ����ȥHCl��
�ʴ�Ϊ����a��bװ��֮���һʢ�б���ʳ��ˮ��ϴ��ƿ����ȥHCl��
����������ǿ�����ԣ���������������Ϊ�����ӣ�������������ΪBr2����������������Һ��Fe2+��Br-ȫ������������Ӧ���ӷ���ʽΪ��2 Fe2++4Br-+3Cl2=6Cl-+2 Fe3++2Br2��
�ʴ�Ϊ��2 Fe2++4Br-+3Cl2=6Cl-+2 Fe3++2Br2��
�������ԡ�����ͼ�⡱����ʽ����Ԫ�ص��ʼ��仯��������ʡ��������Ʊ�ʵ�飬�漰���û�ѧ���������ԭ��Ӧ�ȣ��Ѷ��еȣ����ݵ�������ص㣬�ƶ�A��ͻ�ƿ������Ĺؼ���

��ϰ��ϵ�д�
 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
�����Ŀ