题目内容
6.一定温度下可逆反应N2(g)+3H2(g)?2NH3(g) 达平衡的标志是( )| A. | v正(N2)=$\frac{1}{3}$v正(H2) | B. | v正(N2)=3v逆(H2) | C. | v正(H2)=$\frac{3}{2}$v逆(NH3) | D. | v正(H2)=$\frac{2}{3}$v逆(NH3) |
分析 可逆反应中正逆反应速率相等时该反应达到平衡状态,反应速率之比等于其化学计量数之比,据此分析解答.
解答 解:A.v正(N2)=$\frac{1}{3}$v正(H2),都是正反应速率,其速率之比始终等于化学计量数之比,不能说明反应达到平衡状态,故A错误;
B.v正(N2)=3v逆(H2)反应速率与其计量数之比不相等,所以各物质的正逆反应速率不相等,则该反应没有达到平衡状态,故B错误;
C.V正(H2)=$\frac{3}{2}$V逆(NH3),反应速率与其计量数之比相等,说明正逆反应速率相等,所以反应达到平衡状态,故C正确;
D.V正(H2)=$\frac{2}{3}$V逆(NH3),反应速率与其计量数之比不相等,所以各物质的正逆反应速率不相等,则该反应没有达到平衡状态,故D错误;
故选C.
点评 本题考查化学平衡状态的判断,只有反应前后改变的物理量才能作为判断依据,再结合同一物质的正逆反应速率相等判断,题目难度不大.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
2.下列各组物质中,互为同分异构体的是( )
| A. | 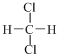 和 和 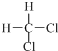 | B. | 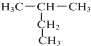 和 和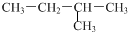 | ||
| C. | CH3CH2CH3和CH2=CHCH3 | D. | 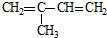 和 和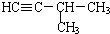 |
17.已知正丁烷的二氯代物有6种同分异构体,则其八氯代物的同分异构体的数目为( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 8种 |
14.下列物质属于离子化合物是( )
| A. | SO2 | B. | H2O | C. | HCl | D. | NaOH |
1.下列5种烃:①2-甲基戊烷 ②2,2-二甲基丙烷 ③己烷 ④庚烷 ⑤戊烷,按它们的沸点由高到低的顺序排列正确的是( )
| A. | ①>②>③>④>⑤ | B. | ②>③>⑤>④>① | C. | ④>③>②>①>⑤ | D. | ④>③>①>⑤>② |
11.下列分子属于手性分子的是( )
| A. | H2O | B. |  | C. |  | D. | H2N-CH2-COOH |
15.下列有关碱金属的说法正确的是( )
| A. | 碱金属元素随原子序数的递增原子半径逐渐减小 | |
| B. | 碱金属元素随原子序数的递增离子氧化性逐渐减弱 | |
| C. | 碱金属元素的单质在氧气点燃都生成过氧化物 | |
| D. | 碱金属元素随原子序数的递增最高价氧化物对应的水化物碱性逐渐减弱 |
16.如图表示可逆反应 mA(g)+nB(g)═pC(g)+qD(g),在不同温度(T)和压强(P)下生成物D的体积分数w(D)随时间的变化情况.关于上述正反应的判断正确的是( )

| A. | P2>P1,m+n>p+q | B. | P1>P2,m+n>p+q | C. | T1>T2,△H<0 | D. | T2>T1,△H>0 |