题目内容
有一铁粉和氧化铜的混合物6.96g,进行如下实验:

根据实验所得数据,关于混合物相关说法正确的是( )
A.生成气体质量为0.2g
B.原混合物中铁的质量分数无法计算
C.实验中反应的H2SO4质量为10.78g
D.原混合物中铜元素的质量不一定为0.64g
A、C
【解析】
试题解析:由题意分析可知:可燃性气体为氢气,浅绿色溶液为硫酸亚铁溶液,红色固体为金属铜。A、由以上分析可计算出CuO的质量是0.80g,Fe的质量是6.16g,其中用于置换出铜的Fe是0.56g,用于和稀硫酸反应置换出氢气的Fe是5.60g,因此生成的气体的质量为0.2g,正确;B、Fe的质量是6.16g,所以可以计算出铁的质量分数,错误;C、最终的溶液是硫酸亚铁溶液,由元素守恒可知:Fe~ FeSO4~H2SO4,所以反应的硫酸质量为10.78g,正确;D、原混合物中铜元素的质量也即铜单质的质量为0.64g,错误,答案选A、C。
考点:考查学生对问题的分析能力及简单计算能力

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如图是测定铝粉(含镁粉)的纯度的实验装置。所用的NaOH(足量)的物质的量浓度为4.5 mol·L-1。不同时间电子天平的读数如下表所示:
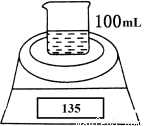
实验操作 | 时间/min | 电子天平的读数/g |
烧杯+NaOH溶液 | 0 | 120 |
烧杯+NaOH溶液+样品 | 0 | 135 |
1 | 134.5 | |
2 | 134.1 | |
3 | 133.8 | |
4 | 133.8 |
(1)反应中生成气体的质量 g。
(2)试计算样品中铝的质量分数。(写出解题过程)
(3)反应后溶液(溶液的体积变化忽略)的c(OH-)。(写出解题过程)