题目内容
对H2O的电离平衡不产生影响的粒子是( )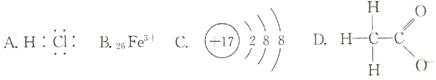
C
解析试题分析:A.HCl溶于水电离产生H+,对水的电离平衡起抑制作用。错误。B.Fe3+在水中发生水解反应:Fe3++3H2O Fe(OH)3(胶体)+3H+;由于消耗了水电离产生的OH-,促进了水的电离,所以水的电离平衡正向移动,直至达到新的平衡。错误。C.Cl-既不会和H+发生作用,也不会与OH-发生反应,因此对水的电离平衡无影响。正确。D.CH3COO-是弱酸根,会发生水解反应:CH3COO-+H2O
Fe(OH)3(胶体)+3H+;由于消耗了水电离产生的OH-,促进了水的电离,所以水的电离平衡正向移动,直至达到新的平衡。错误。C.Cl-既不会和H+发生作用,也不会与OH-发生反应,因此对水的电离平衡无影响。正确。D.CH3COO-是弱酸根,会发生水解反应:CH3COO-+H2O CH3COOH+OH-。由于消耗了水电离产生的H+,,促进了水的电离,所以水的电离平衡正向移动,直至达到新的平衡。错误。
CH3COOH+OH-。由于消耗了水电离产生的H+,,促进了水的电离,所以水的电离平衡正向移动,直至达到新的平衡。错误。
考点:考查影响水的电离平衡的因素的知识。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
已知某温度下CH3COOH和NH3?H2O 的电离常数相等,现向10mL浓度为0.1mol?L?1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中
| A.水的电离程度始终增大 |
| B.c(NH4+)/c(NH3?H2O)先增大再减小 |
| C.c(CH3COOH)与c(CH3COO?)之和始终保持不变 |
| D.当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO?) |
25℃时,下列各溶液(均为0.1 mol·L-1)中,离子(或分子)的物质的量浓度关系正确的是
| A.氯化铵溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B.碳酸钠溶液中:c(HCO3-)+c(CO32-)+c(H2CO3)=0.1 mol·L-1 |
| C.醋酸钠溶液中:c(OH-)>c(H+)+c(CH3COOH) |
| D.碳酸氢钠溶液中:c(Na+)-c(OH-)=c(HCO3-)+c(CO32-)-c(H+) |
常温下关于0.l mol·L-1氯化铵溶液的说法错误的是( )
| A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) | B.加入氨水至pH=7, c(NH4+)>c(C1-) |
| C.滴加浓盐酸可能有,c(NH4+) = c(H+) | D.加入少量CH3COONa固体,c(NH4+)减小 |
下列有关实验的叙述正确的是
| A.已知Cu2O+2H+=Cu2++Cu+H2O,氢气还原氧化铜后生成的红色固体能完全溶于稀硝酸,说明还原产物是铜 |
| B.在中和热测定的实验中,将NaOH溶液和盐酸混合反应后的冷却温度作为末温度 |
| C.仅用淀粉溶液、稀硫酸、碘水、新制氢氧化铜四种试剂可完成淀粉水解产物及水解程度检验的探究实验 |
| D.向盛有少量Mg(OH )2悬浊液的试管中滴加氯化铵溶液,可以看到沉淀溶解 |
相同体积的pH=3的强酸溶液和弱酸溶液分别跟足量的镁完全反应
| A.强酸溶液产生较多的氢气 | B.两者产生等量的氢气 |
| C.无法比较两者产生氢气的量 | D.弱酸溶液产生较多的氢气 |
常温下,0.1mol/L的氨水pH=11,下列叙述错误的是
| A.向该溶液中加水稀释:c(OH—)/c(NH3·H2O )增大 |
| B.0.lmol/L氨水与0.lmol/LH2SO4溶液等体积混合后所得溶液中:c(NH4+)+c(H+)=2c(SO42—)+c(OH—) |
| C.0.1mol/L氨水与0.05mol/LHCl溶液等体积混合后所得溶液中:c(NH4+)+n(NH3)+n(NH3·H2O)=2n(Cl—) |
| D.浓度均为0.1mol/L氨水和NH4Cl溶液等体积混合后,若溶液呈碱性,则 |
有关电解质溶液的叙述,下列说法中正确的是
A.0.2 mol·L-1氨水中,c(OH-)与c(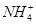 )相等 )相等 |
| B.10 mL 0.02 mol·L-1 HCl溶液与10 mL 0.02 mol·L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12 |
| C.0.1 mol/L的Na2S溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
| D.pH=3的一元酸和pH=11的一元碱等体积混和后的溶液中一定是c(OH-)=c(H+) |