题目内容
【题目】如图为相互串联的甲乙两电解池.
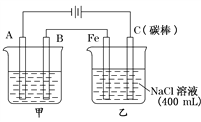
试回答:
(1)甲池若为用电解原理精炼铜的装置,A是________极,材料是________,电极反应为_______,B是________极,材料是________,主要电极反应为__________,电解质溶液为________.
(2)乙池中若滴入少量酚酞试液,电解一段时间后Fe极附近呈________色.
(3)若甲池中阴极增重12.8g,则乙池中阳极放出的气体在标准状况下的体积为________.若此时乙池剩余液体为400 mL,则电解后得到碱液的物质的量浓度为________
【答案】 阴 纯铜 Cu2++2e-===Cu 阳 粗铜 Cu-2e-=Cu2+ CuSO4(其它合理也可以) 红 4.48 L 1.0 mol/L
【解析】结合装置图,与电源负极相连的是阴极,与电源正极相连的是阳极,甲池若为用电解原理精炼铜的装置,则A是阴极,材料为纯铜,发生电极反应是Cu2++2 e- = Cu;B是阳极,材料是粗铜,主要电极反应为:Cu-2e-=Cu2+,电解质溶液为含有铜离子的CuSO4溶液;(2)乙池中实质是电解NaCl饱和溶液,C极上放出Cl2,Fe极上生成H2 ,2H2O+2e-=H2↑+2OH-,若滴入少量酚酞试液,电解一段时间后Fe极附近呈红色;(3)若甲池中阴极增重12.8g,则析出12.8g铜,即转移的电子有![]() ×2=0.4mol,则乙池中阳极放出的气体(氢气)在标准状况下的体积为
×2=0.4mol,则乙池中阳极放出的气体(氢气)在标准状况下的体积为![]() ×22.4L/mol=4.48L;产生OH-有0.4mol,若此时乙池剩余液体为400 mL,则电解后得到碱液的物质的量浓度为
×22.4L/mol=4.48L;产生OH-有0.4mol,若此时乙池剩余液体为400 mL,则电解后得到碱液的物质的量浓度为![]() =1.0mol/L。
=1.0mol/L。

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
