题目内容
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程所放出的热量可计算中和热。回答下列问题:
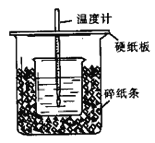
(1)从实验装置上看,图中尚缺少的一种玻璃用品是________________。
(2)烧杯间填满碎纸条的作用__________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 ___________(“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 ________( “变多”“变少”“不变”),所求中和热_______(“相等、不相等”)
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会_____________(“偏大”、“偏小”、“无影响”)。
【答案】 环形玻璃棒 尽量防止热量散失 偏小 变少 相等 偏小
【解析】试题分析:(1)为了让液体充分反应,同时减少热量的损失,使用环形玻璃搅拌棒;(2)碎纸条的作用是减少实验过程中热量的损失;(3)根据△H=-cm△t/n(H2O),如果不盖硬纸板,造成热量损失,△t减少,中和热的数值偏小;(4)放出的热量和物质的量成正比,物质的量越多,放出热量越多,因此放出热量是不相等,但中和热不变,因为中和热是稀酸和碱反应生成1mol水,因此中和热与酸碱用量无关,因此是相等;(5)NH3·H2O是弱碱,电离是吸热过程,因此中和热的数值会减小。

练习册系列答案
相关题目