题目内容
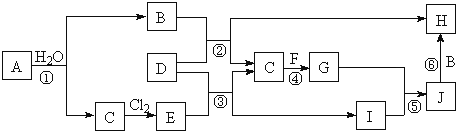
【题目】如图所示各物质是由短周期部分元素组成的单质或其化合物,图中部分反应条件及物质未列出。已知:A、C、D、F均为单质,C、E、F、G常温下是气体,J为白色沉淀,既能溶于B,又能溶于E;物质B、G可以使湿润的红色石蕊试纸变蓝,且B的焰色反应反应呈黄色。反应![]() 是化肥工业的重要反应。
是化肥工业的重要反应。
请回答下列问题:
(1)![]() 的元素在元素周期表中的位置是______,物质B的电子式为______。
的元素在元素周期表中的位置是______,物质B的电子式为______。
(2)上述反应![]() 中,属于化合反应的是______,反应
中,属于化合反应的是______,反应![]() 的离子方程式为______。
的离子方程式为______。
(3)在I的水溶液滴加B溶液至过量的过程中,所观察到的现象为______。
(4)已知G能与![]() 发生置换反应。若以该反应为原理,用石墨作电极构成原电池,负极的电极反应式是______。
发生置换反应。若以该反应为原理,用石墨作电极构成原电池,负极的电极反应式是______。
【答案】第三周期ⅠA族 ![]()
![]()
![]() 有白色沉淀产生,后渐渐溶解至消失
有白色沉淀产生,后渐渐溶解至消失 ![]()
【解析】
转化关系中各物质均为短周期主族元素组成的单质或化合物,常温下气体G可以使湿润的红色石蕊试纸变蓝,则G为NH3,反应④是工业制化肥的重要反应之一,是合成氨,C、F分别为N2、H2中的一种,单质A能与水反应得到B与C,可推知A为Na、B为NaOH、C为H2,故F为N2,Cl2与C反应得到E为HCl,单质D既能与B(NaOH)又能与E(HCl)反应生成C(氢气),故D为Al,H为NaAlO2,I为AlCl3,由反应⑤可知J为Al(OH)3,能溶于盐酸,与氢氧化钠溶液反应得到偏铝酸钠,结合对应物质的性质以及题目要求解答该题。
(1)![]() 为Na,位于周期表第三周期ⅠA族,B为NaOH,由钠离子与氢氧根离子构成,其电子式为
为Na,位于周期表第三周期ⅠA族,B为NaOH,由钠离子与氢氧根离子构成,其电子式为![]() ;
;
(2)框图中,![]() 为钠和水的置换反应,
为钠和水的置换反应,![]() 为铝和氢氧化钠溶液的反应,
为铝和氢氧化钠溶液的反应,![]() 为铝和盐酸的置换反应,
为铝和盐酸的置换反应,![]() 为氢气和氮气的化合反应,生成氨气,
为氢气和氮气的化合反应,生成氨气,![]() 为氨气和氯化铝溶液的复分解反应,
为氨气和氯化铝溶液的复分解反应,![]() 为氢氧化铝与氢氧化钠的反应,则只有
为氢氧化铝与氢氧化钠的反应,则只有![]() 为化合反应,反应
为化合反应,反应![]() 的离子方程式为:
的离子方程式为:![]() ;
;
(3)在氯化铝中加入氢氧化钠溶液,先反应生成白色沉淀氢氧化铝,氢氧化钠过量时,氢氧化铝和氢氧化钠反应生成偏铝酸钠,溶液变澄清,
故答案为:有白色沉淀产生,后渐渐溶解至消失;
(4)![]() 为
为![]() ,与氧气发生置换反应生成氮气,如形成原电池,则负极氨气被氧化生成氮气,电极方程式为
,与氧气发生置换反应生成氮气,如形成原电池,则负极氨气被氧化生成氮气,电极方程式为![]() 。
。

【题目】化学理论较为枯燥,若用化学实验来阐释理论,则会使理论具有趣味性,某班级化学学习小组通过实验室制备CO2的反应探究某些化学理论。下表是实验过程中的数据及相关信息:
序号 | 反应 温度/℃ | c(HCl)/(mol·L-1) | V(HCl)/mL | 10g CaCO3 的形状 | t/min |
① | 20 | 2 | 10 | 块状 | t1 |
② | 20 | 4 | 10 | 块状 | t2 |
③ | 20 | 2 | 10 | 粉状 | t3 |
④ | 40 | 2 | 10 | 粉状 | t4 |
⑤ | 40 | 4 | 10 | 粉状 | t5 |
![]() 表示收集CO2体积为a mL所需的时间。注:气体体积均在相同条件下测得。
表示收集CO2体积为a mL所需的时间。注:气体体积均在相同条件下测得。
(1)由表中的信息可知,实验的目的是探究__________。
(2)表格中的实验①和实验②是探究_____对化学反应速率的影响。分析表格中的信息可知,影响该化学反应速率的因素还有______________________________。
(3)收集a mLCO2所需的时间最少的是实验______________________________。
【题目】常温下,部分酸的电离平衡常数如下:
化学式 | HF | HCN | H2CO3 |
电离常数 | Ka=3.5×10-4 | Ka=5.0×10-10 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
(1)c(H+)相同的三种酸溶液的浓度从大到小为___。
(2)若HCN溶液的起始浓度为0.01mol·L-1,平衡时c(H+)约为__mol·L-1。使此溶液中HCN的电离程度增大且c(H+)也增大的方法是__。
(3)中和等量的NaOH,消耗等pH的氢氟酸和硫酸的体积分别为aL、bL,则a__(填“大于”“小于”或“等于”,下同)b。中和等浓度、等体积的氢氟酸和硫酸需要NaOH的物质的量为n1、n2,则n1__n2。
(4)向NaCN溶液中通入少量的CO2,发生反应的离子方程式为__。
(5)设计实验证明氢氟酸比HCl的酸性弱__。
【题目】相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:2SO3(g)![]() 2SO2(g)+O2(g)△H=+197kJ/mol。实验测得起始、平衡时的有关数据如下表:
2SO2(g)+O2(g)△H=+197kJ/mol。实验测得起始、平衡时的有关数据如下表:
容器编号 | 起始时各物质物 质 的量 /mol | 平衡时反应中的能量变化 | ||
SO3 | SO2 | O2 | ||
① | 2 | 0 | 0 | 吸收热量akJ |
② | 0 | 2 | 1 | 放出热 量 bkJ |
③ | 4 | 0 | 0 | 吸收热量ckJ |
下列叙述正确的是( )
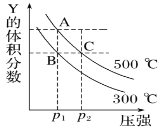
A. 达平衡时O2的体积分数:①>③
B. 热量关系:a一定等于b
C. ①②③ 反应的平衡常数:③>①>②
D. ①中的密度不再改变时说明反应已达到平衡状态