题目内容
【题目】如图为N2(g)和 O2(g)反应生成 NO(g)过程中的能量变化,下列正确的是( )

A.1molN2(g) 和 NA 个 O2(g) 反 应 放 出 的 能 量 为 180 kJ
B.1molN2(g)和 1molO2(g)具有总键能小于 2molNO(g)具有的总键能
C.该反应的热化学方程式为:N2(g)+ O2(g)= 2NO(g)△H=+180 kJmol﹣1
D.吸热反应一定需要加热才能发生
【答案】C
【解析】
化学反应的焓变等于反应物的总键能减去生成物的总键能。
A.根据图中数据可求得△H=946 kJmol﹣1+498 kJmol﹣1-2×623 kJmol﹣1=+180 kJmol﹣1,为吸热反应,所以1molN2(g)和 NA 个O2(g),即1molN2(g)和 1mol O2(g) 反应吸收的能量为 180 kJ,A项错误;
B. 化学反应的焓变等于反应物的总键能减去生成物的总键能,该反应为吸热反应,所以1molN2(g)和 1mol O2(g)大于2mol NO(g)的总键能,B项错误;
C.结合A分析,可推出该反应的热化学方程式为:N2(g)+ O2(g)= 2NO(g) △H=+180 kJmol﹣1,C项正确;
D. 吸热反应不一定需要加热才能发生,比如氢氧化钡晶体和氯化铵晶体的反应,D项错误;
答案选C。

 阅读快车系列答案
阅读快车系列答案【题目】Ⅰ.按要求回答下列问题:
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g)![]() NH2COONH4(s)△H1
NH2COONH4(s)△H1
反应Ⅱ:NH2COONH4(s)![]() CO(NH2)2(s)+H2O(g)△H2=+72.49kJ/mol
CO(NH2)2(s)+H2O(g)△H2=+72.49kJ/mol
总反应:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)△H3=-86.98kJ/mol
CO(NH2)2(s)+H2O(g)△H3=-86.98kJ/mol
①反应Ⅰ的△H1=__。
②一定温度下,在体积固定的密闭容器中按n(NH3):n(CO2)=2:1进行反应Ⅰ,下列能说明反应Ⅰ达到了平衡状态的是__(填序号)。
A.容器内气体总压强不再变化
B.NH3与CO2的转化率相等
C.容器内混合气体的密度不再变化
(2)在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①该反应的化学平衡常数表达式为K=__。
②该反应为__(填“吸热”或“放热”)反应。
③某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为__℃。
④在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2mol·L-1,c(H2)为1.5mol·L-1,c(CO)为1mol·L-1,c(H2O)为3mol·L-1,此时反应向__(填“正向”或“逆向”)进行。
(3)工业上从废铅蓄电池废液回收铅的过程中,常用纯碱溶液与处理后的铅膏(主要含PbSO4)发生反应:PbSO4(s)+CO![]() (aq)
(aq)![]() PbCO3(s)+SO
PbCO3(s)+SO![]() ( aq)。
( aq)。
已知溶度积常数:Ksp(PbSO4)=1.6×10-8,Ksp(PbCO3)=7.4×10-14,则该反应的化学平衡常数K=__。
Ⅱ.N2H4—O2燃料电池是一种高效低污染的新型电池,其装置如图所示:
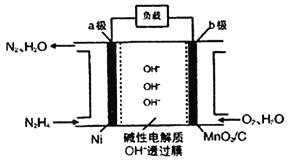
(1)N2H4的电子式为__;
(2)a极的电极反应方程式为___。