题目内容
【题目】(1)卤族元素组成的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识它们。

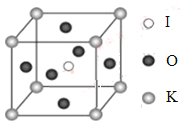
①如图1为碘晶体的晶胞结构。有关说法正确的是_________(填序号)。
a.平均每个晶胞中有4个碘分子
b.平均每个晶胞中有4个碘原子
c.碘晶体为无限延伸的空间结构,是原子晶体
d.碘晶体中存在的相互作用有非极性键和范德华力
②已知CaF2晶胞(图2)的密度为ρ g/cm3,NA表示阿伏加德罗常数的值,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的摩尔质量可表示为_________________。
(2)以MgCl2为原料用电解熔融盐法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外,还有_______________。
(3)有研究表明,化合物X可用于研究模拟酶,当结合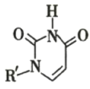 或Cu(I)(I表示化合价为+1)时,分别形成如下图所示的A和B:
或Cu(I)(I表示化合价为+1)时,分别形成如下图所示的A和B:

①A中连接相邻含N杂环的碳碳键可以旋转,说明该碳碳键具有_________键的特性。
②微粒间的相互作用包括化学键和分子间相互作用,比较A和B中微粒间相互作用力的差异:________________。
【答案】ad ![]() g/mol 增强熔融盐的导电性 σ A 中存在分子间氢键,B中存在配位键
g/mol 增强熔融盐的导电性 σ A 中存在分子间氢键,B中存在配位键
【解析】
(1)①a.碘晶体的构成微粒是I2,I2位于晶胞的顶点和面心上,所以一个晶胞中含有的I2分子数目为8×![]() +6×
+6×![]() =4,a正确;
=4,a正确;
b. 根据选项a分析可知一个晶胞中含有4个I2分子,则含有的I原子数目为4×2=8个,b错误;
c. 碘晶体为无限延伸的空间结构,构成微粒为分子,属于分子晶体,c错误;
d. 碘晶体中的I2分子内碘原子间存在I-I为非极性键,且晶体中分子之间存在范德华力,故碘晶体中存在的相互作用有非极性键和范德华力,d正确;
故合理选项是ad;
②该晶胞中含有Ca2+的个数为![]() ,氟离子的个数为8×1=8,一个晶胞中含有4个CaF2,晶胞体积V=a3 cm3,CaF2密度ρ g/cm3,ρ=
,氟离子的个数为8×1=8,一个晶胞中含有4个CaF2,晶胞体积V=a3 cm3,CaF2密度ρ g/cm3,ρ=![]() ,则CaF2的摩尔质量=
,则CaF2的摩尔质量=![]() g/mol,故M相对分子质量
g/mol,故M相对分子质量![]() ;
;
(2)离子浓度越大,其熔融盐的导电性越强,所以MgCl2为原料用电解熔融盐法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外,还有增大离子浓度,从而增大熔融盐的导电性;
(3)①根据σ键是共价单键,可以旋转,而π键不能旋转,根据A中连接相邻含N杂环的碳碳键可以旋转,说明该碳碳键具有σ键的特点;
②根据图片知,A中含有氢键,B中含有配位键,则A和B中微粒间相互作用力的差异是A中含有氢键,B中含有配位键。