题目内容
【题目】运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
I.氨为重要的化工原料,有广泛用途。
(1)合成氨中的氢气可由下列反应制取:
a. CH4(g)+H2O(g)CO(g)+3H2(g) H1=+216.4kJ/mol
b. CO(g)+H2O(g)CO2(g)+H2(g) H2=-41.2kJ/mol
则反应CH4(g)+2H2O(g)CO2(g)+4H2(g) H= _____________。
(2)起始时投入氮气和氢气的物质的量分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度的关系如图。

①恒压时,反应一定达到平衡状态的标志是_____________(填序号)
A.![]() 和
和![]() 的转化率相等 B.反应体系密度保持不变
的转化率相等 B.反应体系密度保持不变
C.![]() 保持不变 D.
保持不变 D.![]()
②P1_____P2 (填“>”“=”或“不确定”,下同);反应的平衡常数:B点_______D点。
③C点![]() 的转化率为________;在A、B两点条件下,该反应从开始到平衡时生成氮气的平均速率:υ(A)__________υ(B)。
的转化率为________;在A、B两点条件下,该反应从开始到平衡时生成氮气的平均速率:υ(A)__________υ(B)。
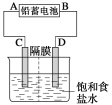
Ⅱ.用间接电化学法去除烟气中NO的原理如下图所示。
已知阴极室溶液呈酸性,则阴极的电极反应式为_____________。反应过程中通过质子交换膜(ab)的![]() 为2mol时,吸收柱中生成的气体在标准状况下的体积为_____________L。
为2mol时,吸收柱中生成的气体在标准状况下的体积为_____________L。

【答案】+175.2kJ/mol BC < > 66.7% < 2SO32-+4H++2e-=S2O42-+2H2O 11.2
【解析】
I.(1)则将a+b可得CH4(g)+2H2O(g)CO2(g)+4H2(g) △H;
(2)①起始时投入氮气和氢气分别为1mol、3mol,在不同温度和压强下合成氨,达到平衡时,正、逆反应速率相等,各物质的浓度不变,气体的总物质的量不变,以此判断;
②增大压强,平衡正向移动,平衡混合气体中氨气的百分含量增大;升高温度,平衡逆向移动,平衡常数减小;
③起始时投入氮气和氢气分别为1mol、3mol,反应的方程式为N2(g)+3H2(g)2NH3(g),C点氨气的含量为50%,结合方程式计算;压强越大、温度越高,反应速率越快;
II.根据图示可知,阴极通入的SO32-发生得电子的还原反应生成S2O42-,结合溶液为酸性书写阴极反应式;写出电解池的总反应,根据通过的氢离子物质的量可知转移电子的物质的量,吸收柱中生成的气体为氮气,然后利用电子守恒计算氮气的物质的量,最后根据V=nVm计算标况下体积。
I.(1)已知a.CH4(g)+H2O(g)CO(g)+3H2(g)△H=+216.4kJ/mol
b.CO(g)+H2O(g)CO2(g)+H2(g)△H=-41.2kJ/mol
则将a+b,可得CH4(g)+2H2O(g)CO2(g)+4H2(g) △H=(+216.4-41.2)kJ/mol=+175.2kJ/mol;
(2)①A.N2和H2的起始物料比为1:3,且按照1:3反应,则无论是否达到平衡状态,转化率都相等,N2和H2转化率相等不能用于判断是否达到平衡状态,A错误;
B.气体的总质量不变,由于该反应的正反应是气体体积减小的反应,恒压条件下,当反应体系密度保持不变时,说明体积不变,则达到平衡状态,B正确;
C.![]() 保持不变,说明氢气、氨气的浓度不变,反应达到平衡状态,C正确;
保持不变,说明氢气、氨气的浓度不变,反应达到平衡状态,C正确;
D.达平衡时各物质的浓度保持不变,但不一定等于化学计量数之比,![]() 不能确定反应是否达到平衡状态,D错误;
不能确定反应是否达到平衡状态,D错误;
故合理选项是BC;
②由于该反应的正反应是气体体积减小的反应,增大压强,平衡正向移动,平衡混合气体中氨气的百分含量增大,由图象可知P1<P2,该反应的正反应是放热反应,升高温度,平衡逆向移动,平衡常数减小,则反应平衡常数:B点>D点;
③起始时投入氮气和氢气分别为1mol、3mol,反应的方程式为N2(g)+3H2(g)2NH3(g),C点氨气的含量为50%,设转化N2物质的量为xmol,则
N2(g) +3H2(g) 2NH3(g)
起始:1mol 3mol 0
转化:x mol 3xmol 2xmol
平衡:(1-x)mol (3-3x)mol 2xmol
则![]() ×100%=50%,解得x=
×100%=50%,解得x=![]() ,则C点H2的转化率为
,则C点H2的转化率为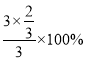 =66.7%,B点的压强、温度都比A点高,压强越大、温度越高,反应速率越大,所以υ(A)<υ(B);
=66.7%,B点的压强、温度都比A点高,压强越大、温度越高,反应速率越大,所以υ(A)<υ(B);
II.根据图示可知,阴极通入的SO32-发生得电子的还原反应生成S2O42-,则阴极反应式为:2SO32-+4H++2e-=S2O42-+2H2O;电解池的阳极水电离出的氢氧根离子放电生成氧气,发生反应为:2H2O-4e-=4H++O2↑,则电解池中总反应为:4SO32-+4H+![]() 2S2O42-+2H2O+O2↑,即转移4mol电子时有4mol氢离子通过质子交换膜,则反应过程中通过质子交换膜(ab)的H+为2mol时,转移电子的物质的量为2mol,生成1molS2O42-,图示NO吸收柱中S2O42-失去电子被氧化成SO32-,NO得到电子被还原成N2,根据得失电子守恒可知,吸收柱中生成N2的物质的量为:n(N2)=
2S2O42-+2H2O+O2↑,即转移4mol电子时有4mol氢离子通过质子交换膜,则反应过程中通过质子交换膜(ab)的H+为2mol时,转移电子的物质的量为2mol,生成1molS2O42-,图示NO吸收柱中S2O42-失去电子被氧化成SO32-,NO得到电子被还原成N2,根据得失电子守恒可知,吸收柱中生成N2的物质的量为:n(N2)=![]() =0.5mol,标况下0.5mol氮气的体积为:22.4L/mol×0.5mol=11.2L。
=0.5mol,标况下0.5mol氮气的体积为:22.4L/mol×0.5mol=11.2L。

 习题精选系列答案
习题精选系列答案【题目】工业酸性废水中的![]() 可转化为
可转化为![]() 除去,实验室用电解法模拟该过程,结果如下表所示(实验开始时溶液体积为
除去,实验室用电解法模拟该过程,结果如下表所示(实验开始时溶液体积为![]() 的起始浓度、电压、电解时间均相同),下列说法中,不正确的是( )
的起始浓度、电压、电解时间均相同),下列说法中,不正确的是( )
实验 | ① | ② | ③ |
电解条件 | 阴、阳极均为石墨 | 阴、阳极均为石墨,滴加 | 阴极为石墨,阳极为铁,滴加 |
| 0.922 | 12.7 | 57.3 |
A. 对比实验①②可知,降低pH可以提高![]() 的去除率
的去除率
B. 实验②中,![]() 在阴极放电的电极反应式是
在阴极放电的电极反应式是![]()
C. 实验③中,![]() 去除率提高的原因是阳极产物还原
去除率提高的原因是阳极产物还原![]()
D. 实验③中,理论上电路中每通过![]() 电子,则有
电子,则有![]()
![]() 被还原
被还原