题目内容
下图是将SO2转化为重要的化工原料H2SO4的原理示意图,下列说法不正确的是( )
| A.该装置将化学能转化为电能 |
| B.催化剂b表面O2发生还原反应,其附近酸性增强 |
| C.催化剂a表面的反应是SO2+2H2O-2e-=SO42-+4H+ |
| D.若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为8∶15 |
B
解析

练习册系列答案
相关题目
肼(N2H4)——空气燃料电池是一种环保型碱性燃料电池,电解质为20%~30%的KOH溶液,电池总反应为N2H4+ O2=N2+2H2O。下列关于该电池工作时说法中正确的是
| A.溶液的pH保持不变 |
| B.溶液中的阴离子向正极移动 |
| C.正极的电极反应式:O2+4H++4e—=2H2O |
| D.负极的电极反应式:N2H4+4OH—﹣4e— =4H2O +N2 |
铅蓄电池的反应原理为:2PbSO4+2H2O Pb+PbO2+2H2SO4,下列叙述中,正确的是
Pb+PbO2+2H2SO4,下列叙述中,正确的是
| A.PbSO4的氧化性比PbO2的强、还原性比Pb的强 |
| B.放电时,PbO2为氧化剂、做负极,Pb为还原剂、做正极 |
| C.放电时,当有2 mol H2SO4反应时,会有1.204×1024个电子从铅电极流出 |
| D.充电时,PbSO4既被氧化又被还原,Pb是阳极产物之一 |
用石墨作电极,电解下列物质的溶液,其实质不是电解水的是( )
| A.NaNO3 | B.NaOH | C.Na2SO4 | D.NaCl |
某小组利用下列装置进行电化学实验,下列实验操作及预期现象正确的是( )
| A.X和Y与电流表连接,电子由Cu极流向Zn极 |
| B.X和Y与电流表连接,将Zn换成Fe测得电流更大 |
| C.X和Y分别与电源“-”、“+”极相连,Cu极质量减轻 |
| D.X和Y分别与电源“-”、“+”极相连,Zn极质量减轻 |
结合下图判断,下列叙述正确的是( )
| A.Ⅰ和Ⅱ中正极均保护 |
| B.Ⅰ和Ⅱ中负极反应均是Fe-2e-=Fe2+ |
| C.Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-=4OH- |
| D.Ⅰ和Ⅱ中分别加入少量K3[Fe(CN)6]溶液,均有蓝色沉淀 |
固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体。这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体。目前固体电解质在制造全固态电池及其他传感器、探测器等方面的应用日益广泛。如RbAg4I5晶体,其中迁移的物种全是Ag+,室温导电率达0. 27 Ω-1·cm-1。利用RbAg4I5晶体,可以制成电化学气敏传感器。下图是一种测定O2含量的气体传感器示意图,被分析的O2可以透过聚四氟乙烯薄膜,由电池电动势变化可以得知O2的含量。在气体传感器工作过程中,下列变化肯定没有发生的是( )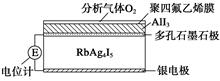
| A.I2+2Rb++2e-=2RbI |
| B.I2+2Ag++2e-=2AgI |
| C.Ag-e-=Ag+ |
| D.4AlI3+3O2=2Al2O3+6I2 |
化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如下图所示,计算反应4~8 min 间的平均反应速率和推测反应16 min 时反应物的浓度,结果应是( )。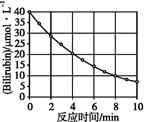
| A.2.5 μmol·L-1·min-1和2.0 μmol·L-1 |
| B.2.5 μmol·L-1·min-1和2.5 μmol·L-1 |
| C.3.0 μmol·L-1·min-1和3.0 μmol·L-1 |
| D.5.0 μmol·L-1·min-1和3.0 μmol·L-1 |
a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块如图所示放置一段时间。下列有关描述错误的是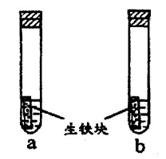
| A.生铁块中的碳是原电池的正极 |
| B.a试管内压强变大,b试管内压强变小 |
C.两试管中相同的电极反应式是:2Fe Fe2++2e- Fe2++2e- |
| D.两试管中均发生了电化腐蚀 |