题目内容
【题目】如何用所提供的试剂和方法除去各粉末状混合物中的杂质(括号内为杂质)。将所选答案的编号填在表中相应的空格内。
可供选择的试剂:A.盐酸 B.NaOH溶液 C.O2 D.水 E.不用其他试剂
可选用的操作:①水洗 ②加热 ③过滤 ④结晶
粉末状混合物 | 所选试剂 | 所选操作 | |
(1) | CaCO3(SiO2) | ______ | ______ |
(2) | NaCl(SiO2) | ______ | ______ |
(3) | SiO2(Fe2O3) | ______ | ______ |
(4) | SiO2(CaCO3) | ______ | ______ |
(5) | SiO2(Si) | ______ | ______ |
(6) | SiO2(H2SiO3) | ______ | ______ |
【答案】B ③ D ③④ A ③ A ③ C ② E ②
【解析】
(1)除去CaCO3中的SiO2可用NaOH溶液,溶解SiO2后再过滤,SiO2+2NaOH=Na2SiO3+H2O,故答案为:B;③;
(2)除去NaCl中的SiO2可先溶于水,再过滤、结晶,因NaCl溶于水而SiO2不溶于水,故答案为:D;③④
(3)Fe2O3+6HCl=2FeCl3+3H2O,故答案为:A;③;
(4)除去SiO2中的CaCO3可用盐酸溶解,然后再过滤,CaCO3+2HCl=CaCl2+CO2↑+H2O,故答案为:A;③;
(5)除去SiO2中的Si可用加热法:Si+O2![]() SiO2,故答案为:C;②;
SiO2,故答案为:C;②;
(6)除去SiO2中的H2SiO3可用加热法:H2SiO3![]() H2O+SiO2,故答案为:E;②。
H2O+SiO2,故答案为:E;②。

【题目】实验室铝热反应的实验装置如下:
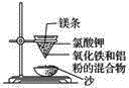
(1)下面放置盛细沙的____________(填名称)。
(2)镁条的作用是______________________________________。
(3)实验现象有:
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________。
(4)写出该反应的化学反应方程式:________________,在冶金工业上也常用这一反应原理来冶炼________。
A.不活泼金属 B.较活泼金属
C.稀有金属 D.高熔点金属
(5)已知下表数据:
物质 | Al | Al2O3 | Fe | Fe2O3 |
熔点/℃ | 660 | 2054 | 1535 | 1462 |
沸点/℃ | 2467 | 2980 | 2750 |
①某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是该反应放出的热量能使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理?________(填“合理”或“不合理”)。
②设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是______________,当观察到___________________现象时,反应的离子方程式是________________________________________________________________________。
③实验室欲溶解此熔融物,最好选用下列试剂中的________(填字母)。
A.浓硫酸 B.稀硫酸
C.稀硝酸 D.NaOH溶液